题目内容
11.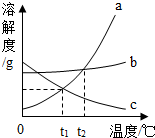 如图是a、b、c三种物质的溶解度曲线,下列叙述正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列叙述正确的是( )| A. | a的溶解度比c大 | |
| B. | a中有少量的c可采用降温结晶的方法提纯 | |
| C. | t2℃时,a、b两种物质饱和溶液中溶质的质量一定相等 | |
| D. | 将t2℃时a、b、c的饱和溶液降温至t1℃,所得溶液中溶质质量分数由大到小的顺序是b>a=c |
分析 A、比较溶解度大小须确定温度;
B、据溶解度曲线可知物质的溶解度随温度变化情况,并分析提纯物质的方法;
C、不知溶液的质量,无法判断所含溶质的质量关系;
D、据三种物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数计算方法分析解答.
解答 解:A、比较溶解度大小须确定温度;
B、a的溶解度随温度升高而增大,且变化较大,c的溶解度随温度升高而减小,所以若a中有少量的c可采用降温结晶的方法提纯,正确;
C、不知溶液的质量,无法判断所含溶质的质量关系,故错误;
D、将t2℃时a、b、c的饱和溶液降温至t1℃,ab析出晶体,c溶液中溶质、溶剂的质量不变,溶质质量分数与降温前相等,据饱和溶液中质量分数=$\frac{溶解度}{溶解度+100g}$×100%,即溶解度越大质量分数也就越大,而t1℃b的溶解度大于a的溶解度大于降温前c 的溶解度,故所得溶液中溶质质量分数由大到小的顺序是b>a>c,故错误;
故选:B.
点评 不同温度下物质的溶解度不同,所以比较溶解度大小须确定温度,饱和溶液中溶解度大则溶质的质量分数大,并能据溶解度曲线分析提纯物质的方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.亲历化学实验话动,可以激发我们学习化学的兴趣,也可以让我们体验探究的过程.请你参与下列实验活.
【实验名称】探究燃烧的条件
【实聢目的】加深对燃烧条件的认识,体验实验探究的过程.
【实验用品】烧杯、玻璃棒,镊子,酒精灯,三脚架、大理石块,铜片,盐酸,酒精,棉花、乒乓球碎片、蜡烛、滤纸
【实验内容】请完成下表内容.
【实验名称】探究燃烧的条件
【实聢目的】加深对燃烧条件的认识,体验实验探究的过程.
【实验用品】烧杯、玻璃棒,镊子,酒精灯,三脚架、大理石块,铜片,盐酸,酒精,棉花、乒乓球碎片、蜡烛、滤纸
【实验内容】请完成下表内容.
| 实验序号 | 实验步骤 | 实验现象 | 实验结论 |
| (1) | 燃烧条件之一:需要可燃物 | ||
| (2) | 燃烧条件之二: | ||
| (3) | 燃烧条件之三: |
20.下列变化中属于物理变化的是( )
| A. | 鞭炮爆炸 | B. | 食物腐败 | C. | 冰雪融化 | D. | 钢铁生锈 |
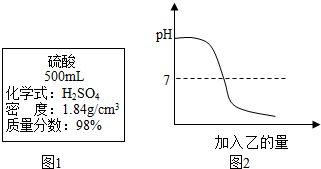 硫酸是重要的化工原料,也是实验室常用的酸.
硫酸是重要的化工原料,也是实验室常用的酸.