题目内容
17.现有五瓶失去标签的溶液A、B、C、D、E,它们分别是氢氧化钠、氯化钠、硫酸铜、氯化钡、稀硫酸中的一种,某同学不用其它试剂,用如下实验加以鉴别.
第一步:通过观察发现E溶液呈蓝色,其它溶液均为无色;
第二步:取少量A、B、C、D溶液,分别滴加E溶液,现象为:A溶液中出现白色沉淀,B溶液中出现
蓝色沉淀,C和D溶液均无明显现象;
第三步:取第二步中产生的蓝色沉淀,滴加C溶液后沉淀消失.
则:(1)A溶液中溶质的化学式是BaCl2;
(2)写出B和E反应的化学方程式:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
分析 根据物质的性质进行分析,硫酸铜溶液是蓝色的,硫酸铜能与氢氧化钠反应生成蓝色沉淀,能与氯化钡反应产生白色沉淀,氯化钡能与硫酸反应生成白色沉淀,据此解答.
解答 解:E溶液为蓝色,则E是硫酸铜;硫酸铜与A混合产生白色沉淀,则A是氯化钡;硫酸铜与B混合产生蓝色沉淀,则B是氢氧化钠;氢氧化铜沉淀能溶于硫酸,加入C,沉淀消失,则C是硫酸,故D是氯化钠;
(1)A是氯化钡,故答案为:BaCl2;
(2)B是氢氧化钠,E是硫酸铜,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故答案为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
点评 本题考查了常见物质的鉴别,完成此题,可以依据物质的性质差异进行分析即可.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
7.表一是氢氧化钙在不同温度下的部分溶解度数值;表二是在20℃时,物质溶解度的相对大小.根据表中信息判断,下列说法正确的是( )
表一:
表二:
表一:
| 温度/℃ | 0 | 10 | 20 |
| 溶解度/g | 0.18 | 0.17 | 0.16 |
| 溶解度/g | <0.01 | 0.01~1 | 1~10 |
| 一般称为 | 难溶 | 微溶 | 可溶 |
| A. | 20℃时,氢氧化钙微溶于水 | |
| B. | 氢氧化钙的溶解度随温度的升高而增大 | |
| C. | 在10℃时,将0.17g氢氧化钙溶于水中一定能得到饱和溶液 | |
| D. | 将质量相等的氢氧化钙加入不同质量的水中,所得溶液的溶质质量分数一定不同 |
8.下列实验操作错误的是( )
| A. | 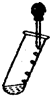 滴加液体 | B. |  稀释浓硫酸 | C. |  盖灭酒精灯 | D. |  H2还原CuO |
12. 某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )
某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )
 某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )
某气体可能含有水蒸气、CO、H2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过如图的装置( )| A. | 丙、甲、丙、乙 | B. | 甲、乙、丙 | C. | 丙、甲、乙、丙 | D. | 丙、甲、乙 |

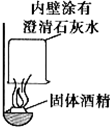 某校化学兴趣小组的同学在一次聚餐中,发现并对燃料固体酒精产生了好奇,于是对其成分进行了探究.
某校化学兴趣小组的同学在一次聚餐中,发现并对燃料固体酒精产生了好奇,于是对其成分进行了探究. 甲、乙、丙三种固体的溶解度曲线如图.将t1℃时甲、丙饱和溶液的试管(均有少量未溶解的固体)放进盛有热水(t2℃)的烧杯里.下列有关说法正确的是( )
甲、乙、丙三种固体的溶解度曲线如图.将t1℃时甲、丙饱和溶液的试管(均有少量未溶解的固体)放进盛有热水(t2℃)的烧杯里.下列有关说法正确的是( )