题目内容
我国制碱工业先驱侯德榜先生发明了“侯氏制碱法”,其模拟流程如图所示:

(1)操作a的名称是________。
(2)X是一种可用作氮肥的盐,其化学式可能是______________。
(3)流程图中可循环利用的物质是__________________。
 过滤NH4ClCO2、H2O
【解析】
(1)操作a实验操作的名称是过滤;
(2)分析图可知:氨气、二氧化碳和食盐水反应生成碳酸氢钠和氯化铵,氯化铵的化学式为:NH4Cl;
(3)由图示可知二氧化碳、水能被循环利用。
过滤NH4ClCO2、H2O
【解析】
(1)操作a实验操作的名称是过滤;
(2)分析图可知:氨气、二氧化碳和食盐水反应生成碳酸氢钠和氯化铵,氯化铵的化学式为:NH4Cl;
(3)由图示可知二氧化碳、水能被循环利用。
下列实验操作正确的是( )
A.  读取液体体积 B.
读取液体体积 B.  液体的倾倒 C.
液体的倾倒 C.  液体的加热 D.
液体的加热 D.  稀释浓硫酸
稀释浓硫酸
 D
【解析】试题A、量筒读数时,视线应该与量筒内凹液面的最低处保持水平,故错误;B、往试管内倾倒液体时,瓶塞倒放桌面,试管要略微倾斜,瓶口紧挨着试管口倾倒,避免液体溅出,故错误;C、给试管内液体加热时,试管内液体的体积不超过试管容积的三分之一,故错误;D、稀释浓硫酸时不能将水倒入浓硫酸中,要将浓硫酸倒入水中,并不断搅拌,防止水浮在浓硫酸的水面上沸腾溅出,故正确;故选D。
D
【解析】试题A、量筒读数时,视线应该与量筒内凹液面的最低处保持水平,故错误;B、往试管内倾倒液体时,瓶塞倒放桌面,试管要略微倾斜,瓶口紧挨着试管口倾倒,避免液体溅出,故错误;C、给试管内液体加热时,试管内液体的体积不超过试管容积的三分之一,故错误;D、稀释浓硫酸时不能将水倒入浓硫酸中,要将浓硫酸倒入水中,并不断搅拌,防止水浮在浓硫酸的水面上沸腾溅出,故正确;故选D。 下列A~ E是初中化学中的五个实验装置,请按要求填空:

(1)图A装置中的无色液体可用于检验氧气中含少量二氧化碳,该反应的化学符号表达式为_______________。
(2)图B所示实验是“铁的锈蚀实验”,观察到的现象:银白色铁丝生锈,同时烧杯中的红墨水被吸入导管中。根据此实验的现象,并结合“热胀冷缩”原理,可知在密封体系内,气压变小的原因可能是____________;气压变大的原因可能是___________。
①密封体系内气体总量增多; ②密封体系内气体总量减少;
③密封体系内的温度升高; ④密封体系内的温度降低。
(3)图C实验说明氧气的体积约占空气的_________,下列操作不妥的是_________。
①实验前检查装置气密性 ②实验前未夹紧止水夹
③冷却至室温后再打开止水夹 ④红磷足量
(4)图D实验的现象为_________________,该实验可以证明水是由_______________组成的。
(5)图E所示实验观察到用石蕊试液染成紫色的纸花变为红色,小花变红的原因是___ (用化学符号表达式表示)。
 CO2+Ca(OH)2=CaCO3+H2O②④①③1/5②发出淡蓝色火焰,放热,产生水雾氢元素和氧元素CO2+H2O=H2CO3
【解析】
(1)检验二氧化碳气体用澄清石灰水,即通入所得气体,若石灰水变浑浊,说明通入的气体是二氧化碳,反应方程式是:Ca(OH)2+CO2=CaCO3↓+H2O;
(2)铁生锈是与氧气和水同时接触,所以实验乙中观察到的现象:银白色铁丝生锈,由于消耗氧...
CO2+Ca(OH)2=CaCO3+H2O②④①③1/5②发出淡蓝色火焰,放热,产生水雾氢元素和氧元素CO2+H2O=H2CO3
【解析】
(1)检验二氧化碳气体用澄清石灰水,即通入所得气体,若石灰水变浑浊,说明通入的气体是二氧化碳,反应方程式是:Ca(OH)2+CO2=CaCO3↓+H2O;
(2)铁生锈是与氧气和水同时接触,所以实验乙中观察到的现象:银白色铁丝生锈,由于消耗氧... 2018年3月,国务院总理李克强在政府工作报告中强调:“坚决打好蓝天保卫战”。 各地积极行动,落实措施。下列做法错误的是( )
A. 积极推广使用新能源公交车
B. 火力发电厂进行脱硫、控尘处理
C. 禁止化石燃料的使用
D. 限制、禁止燃放烟花爆竹
 C
【解析】
A、积极推广使用新能源公交车,可减少污染物排放,利于空气净化,正确;B、火力发电厂进行脱硫、控尘处理,可减少污染物的排放,利于空气净化,正确;C、化石燃料是现代社会的主要能源,可减少使用,不能禁止化石燃料的使用,错误;D、限制、禁止燃放烟花爆竹,可减少空气污染,利于空气净化,正确。故选C。
C
【解析】
A、积极推广使用新能源公交车,可减少污染物排放,利于空气净化,正确;B、火力发电厂进行脱硫、控尘处理,可减少污染物的排放,利于空气净化,正确;C、化石燃料是现代社会的主要能源,可减少使用,不能禁止化石燃料的使用,错误;D、限制、禁止燃放烟花爆竹,可减少空气污染,利于空气净化,正确。故选C。 小茗同学取14%的硫酸溶液70 g于烧杯中,然后向烧杯中慢慢加入10 g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示。
(1)完全反应时共消耗氧化铜的质量是__________。
(2)求反应后所得溶液的溶质质量分数______。
(3)配制14%的硫酸溶液70 g,需要98%的浓硫酸的质量为____________。
 8g20.5%10g
【解析】
(1)氧化铜和硫酸反应生成硫酸铜和水,所以溶液质量增加的就是氧化铜的质量,所以氧化铜的质量=78g-70g=8g;
(2)设当加入49g稀硫酸溶液时恰好完全反应,生成硫酸铜的质量为x,
所以溶液中溶质的质量分数=×100%≈20.5%,
(3)设需要98%的硫酸质量为y,则:70g×14%=y×98%,y=10g。
8g20.5%10g
【解析】
(1)氧化铜和硫酸反应生成硫酸铜和水,所以溶液质量增加的就是氧化铜的质量,所以氧化铜的质量=78g-70g=8g;
(2)设当加入49g稀硫酸溶液时恰好完全反应,生成硫酸铜的质量为x,
所以溶液中溶质的质量分数=×100%≈20.5%,
(3)设需要98%的硫酸质量为y,则:70g×14%=y×98%,y=10g。 下列实验操作能达到实验目的的是(_______)
选项 | 实验目的 | 主要实验操作 |
A | 分离CaO和CaCO3固体的混合物 | 加水充分溶解后,过滤 |
B | 鉴别稀盐酸和NaCl溶液 | 分别加AgNO3溶液 |
C | 除去CaCl2溶液中混有的盐酸 | 加入过量的CaCO3,过滤 |
D | 检验Na2CO3溶液中含有NaOH | 加入足量____________溶液,再滴加酚酞 |
A、A B、B C、C D、D
 CCaCl2(或BaCl2)
【解析】
A、氧化钙与水反应生成氢氧化钙,碳酸钙难溶于水,加水充分溶解后,过滤,无法分离出氧化钙,故选项错误;B、HCl、NaCl都与AgNO3反应生成白色沉淀,无法鉴别,故选项错误;C、HCl能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项正确。故选C。D、Na2CO3溶液与足量Ca...
CCaCl2(或BaCl2)
【解析】
A、氧化钙与水反应生成氢氧化钙,碳酸钙难溶于水,加水充分溶解后,过滤,无法分离出氧化钙,故选项错误;B、HCl、NaCl都与AgNO3反应生成白色沉淀,无法鉴别,故选项错误;C、HCl能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项正确。故选C。D、Na2CO3溶液与足量Ca... 某化学反应的微观示意图如下(一种小球代表一种原子),则下列说法错误的是( )

A. 该反应可以是CH4+Cl2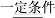 CH3Cl+HCl
CH3Cl+HCl
B. 该反应前后各元素化合价都不变
C. 反应前后原子的种类和数目不变
D. 图中共有4种分子
 B
【解析】
若为氢原子、 为碳原子、 为氯原子,根据质量守恒定律可知,此反应的化学方程式为:CH4+Cl2CH3Cl+HCl。
A、反应的化学方程式为:CH4+Cl2CH3Cl+HCl,故选项正确;B、反应物中各元素的化合价为:氢为+1、碳为-4、氯为0,生成物各元素的化合价为:氢为+1、碳为-4、氯为-1,反应前后氯元素化合价改变了,故选项错误;C、由反应前后分子的结构可知:...
B
【解析】
若为氢原子、 为碳原子、 为氯原子,根据质量守恒定律可知,此反应的化学方程式为:CH4+Cl2CH3Cl+HCl。
A、反应的化学方程式为:CH4+Cl2CH3Cl+HCl,故选项正确;B、反应物中各元素的化合价为:氢为+1、碳为-4、氯为0,生成物各元素的化合价为:氢为+1、碳为-4、氯为-1,反应前后氯元素化合价改变了,故选项错误;C、由反应前后分子的结构可知:... 科学的假设与猜想是探究的先导和价值所在.下列假设引导下的探究肯定没有意义的是( )
A. 探究二氧化碳和水反应可能有硫酸生成
B. 探究钠与水的反应产生的气体可能是氢气
C. 探究镁条表面灰黑色的物质可能只是氧化镁
D. 探究铜丝在酒精灯火焰上灼烧时出现的黑色物质可能是炭黑
 AC
【解析】
根据进行科学探究时,要有合理的理论依据,不能凭空猜测,二氧化碳为酸性氧化物,可以与水反应生成酸,化学反应前后元素的种类不变,钠和水中含有钠元素、氢元素和氧元素,故生成物中含钠元素、氢元素和氧元素,氧化镁为白色固体,镁条表面灰黑色的物质不可能只是氧化镁,铜在灼烧时与空气接触,燃料酒精和空气中都含有碳元素进行分析。
A、二氧化碳为酸性氧化物,可以与水反应生成酸,反应物...
AC
【解析】
根据进行科学探究时,要有合理的理论依据,不能凭空猜测,二氧化碳为酸性氧化物,可以与水反应生成酸,化学反应前后元素的种类不变,钠和水中含有钠元素、氢元素和氧元素,故生成物中含钠元素、氢元素和氧元素,氧化镁为白色固体,镁条表面灰黑色的物质不可能只是氧化镁,铜在灼烧时与空气接触,燃料酒精和空气中都含有碳元素进行分析。
A、二氧化碳为酸性氧化物,可以与水反应生成酸,反应物... 硅是地壳中含量第二的元素,其元素符号为( )
A. S B. Si C. P D. Hg
 B
【解析】
硅是地壳中含量第二的元素,其元素符号Si,故选B。
B
【解析】
硅是地壳中含量第二的元素,其元素符号Si,故选B。 
