题目内容
氮肥硝酸铵的化学式为:NH4NO3,计算:
(1)硝酸铵的相对分子质量.
(2)硝酸铵中各原子的个数比.
(3)硝酸铵中氮元素的质量分数?
(4)140kg的硝酸铵中含有多少千克的氮元素?
(1)硝酸铵的相对分子质量.
(2)硝酸铵中各原子的个数比.
(3)硝酸铵中氮元素的质量分数?
(4)140kg的硝酸铵中含有多少千克的氮元素?
考点:相对分子质量的概念及其计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量为组成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据1个硝酸铵分子构成的进行分析解答.
(3)根据化合物中元素的质量分数=
×100%,进行分析解答.
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答
(2)根据1个硝酸铵分子构成的进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答
解答:解:(1)硝酸铵的相对分子质量为14+1×4+14+16×3=80.
(2)一个硝酸铵分子是由2个氮原子、4个氢原子、3个氧原子构成的,故硝酸铵中N、H、O三种元素的原子个数比为2:4:3.
(3)硝酸铵中氮元素的质量分数为
×100%=35%.
(4)140kg的硝酸铵中含有氮元素的质量为140kg×35%=49kg.
故:(1)硝酸铵的相对分子质量为80;(2)硝酸铵中N、H、O三种元素的原子个数比为2:4:3;(3)硝酸铵中氮元素的质量分数为35%;(4)140kg的硝酸铵中含有49千克的氮元素.
(2)一个硝酸铵分子是由2个氮原子、4个氢原子、3个氧原子构成的,故硝酸铵中N、H、O三种元素的原子个数比为2:4:3.
(3)硝酸铵中氮元素的质量分数为
| 14×2 |
| 80 |
(4)140kg的硝酸铵中含有氮元素的质量为140kg×35%=49kg.
故:(1)硝酸铵的相对分子质量为80;(2)硝酸铵中N、H、O三种元素的原子个数比为2:4:3;(3)硝酸铵中氮元素的质量分数为35%;(4)140kg的硝酸铵中含有49千克的氮元素.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
某物质R在空气中燃烧的化学方程式为R+2O2=CO2+2H2O,根据质量守恒定律,R的化学式是( )
| A、CH4 |
| B、C2H2 |
| C、C2H4 |
| D、C2H2O |
根据金属活动性顺序判断,下列物质之间不能发生化学反应的是( )
| A、铁和硫酸铜溶液 |
| B、铜和稀盐酸 |
| C、锌和硝酸汞溶液 |
| D、镁和稀硫酸 |
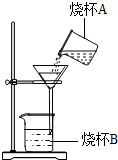 杜雨佳学习了教材26页净化天然水的实验探究后,兴趣浓厚.假期的一天她与几个好朋友去乡村游玩时,用瓶装了一些黄泥水,带回实验室,在老师的指导下,进行实验,制取蒸馏水.请回答下列问题:
杜雨佳学习了教材26页净化天然水的实验探究后,兴趣浓厚.假期的一天她与几个好朋友去乡村游玩时,用瓶装了一些黄泥水,带回实验室,在老师的指导下,进行实验,制取蒸馏水.请回答下列问题: 根据下列仪器,回答问题.
根据下列仪器,回答问题.