题目内容
11.现取某大理石样品(杂质不反应,也不溶于水)14.1g放入烧杯中,再加入100g的稀盐酸,恰好完全反应后所得溶液的质量为105.6g,该大理石中碳酸钙的质量为( )| A. | 10g | B. | 7.3g | C. | 4.4g | D. | 14.4g |
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由质量守恒定律,溶液增加的质量为碳酸钙与二氧化碳的质量差,据此结合差量法进行分析解答.
解答 解:设参加反应的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑ 溶液质量增加的量
100 44 100-44=56
x 105.6g-100g=5.6g
$\frac{100}{56}=\frac{x}{5.6g}$ x=10g
故选:A.
点评 本题难度不大,考查利用化学方程式的计算,利用液体差量法是正确解答本题的关键和捷径.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
1.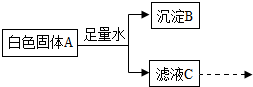 某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:
某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:
完成下列填空:
①操作 I是过滤.根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,C中一定含有的溶质是氯化钠.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
 某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:
某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:完成下列填空:
①操作 I是过滤.根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,C中一定含有的溶质是氯化钠.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表.
| 实验操作 | 现象 | 结论 |
| 向滤液C中加入足量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞 | 无色酚酞变红色 | A中有氢氧化钠 |
19.下列关于实验操作的说法中,不合理的是( )
| A. | CO还原氧化铁实验开始时,先通CO,后加热 | |
| B. | 把98%的浓硫酸沿器壁注入盛有水的量筒内稀释 | |
| C. | 做铁丝在氧气中的燃烧实验时,预先在集气瓶底铺一层细沙 | |
| D. | 过滤时漏斗的末端要紧靠烧杯内壁 |
6.如图是金刚石、石墨、C60、碳纳米管结构示意图,下列说法正确的是( )
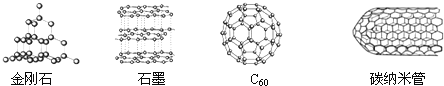

| A. | 这四种物质 都很软,可作润滑剂 | |
| B. | 这四种物质碳原子的排列方式相同 | |
| C. | 这四种物质的结构中都是每个碳原子连接3个碳原子 | |
| D. | 这四种物质完全燃烧后的产物都是CO2 |
12.下列反应中,既是化合反应又是氧化反应的是( )
| A. | 蜡烛+氧气$\stackrel{点燃}{→}$二氧化碳+水 | |
| B. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | |
| C. | 碳酸钙$\stackrel{高温}{→}$氧化钙+二氧化碳 | |
| D. | 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 |
9.我国探月工程已经发现月球中含有种类繁多的矿物,其中有的是在地球上未曾发现过的矿产.下列月球矿物中属于化合物的是( )
| A. | 钛铁矿 | B. | 铁锡合金 | C. | 纯铁 | D. | 硫化银 |
10.下列物质用途不合理的是( )
| A. | 肥皂水用于鉴别硬水和软水 | B. | 活性炭用于除去冰箱内的异味 | ||
| C. | 食用纯碱用于治疗胃酸过多 | D. | 可降解塑料用于制作一次性餐具 |