题目内容
3.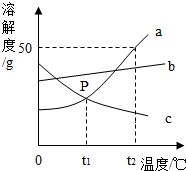 根据图中a、b、c三种固体物质的溶解度曲线,回答下列问题:
根据图中a、b、c三种固体物质的溶解度曲线,回答下列问题:(1)t2℃,a的物质的溶解度为50g.
(2)t1℃时,将接近饱和的c物质的变成该物质的饱和溶液,可采用加入c物质(或升高温度、蒸发水).(任填一种方法即可)
(3)t2℃时.将a、b、c三种物质的饱和溶液,分别降溫至t1℃时,所得溶液中溶质质置分数的大小关系是C.
A.a>b>c B.b>a=c C.b>a>c.
分析 (1)据溶解度曲线可知某温度下物质的溶解度;
(2)不饱和溶液变为饱和溶液的一般方法是加入溶质、蒸发溶剂、降温;
(3)据饱和溶液溶质的质量分数计算方法及物质的溶解度随温度变化情况分析解答.
解答 解:(1)由图可知:t2℃时a的物质的溶解度为50g;
(2)c的溶解度随温度升高而减小,所以t1℃时,将接近饱和的c物质的变成该物质的饱和溶液,可采用 加入c物质、蒸发溶剂、升高温度的方法;
(3)t2℃时.将a、b、c三种物质的饱和溶液,分别降溫至t1℃时,ab的溶解度减小,析出晶体,但依然是饱和溶液,溶质的质量分数减小,c的溶解度变大,溶质、溶剂的质量不变,溶质的质量分数与降温前相等;饱和时溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,即溶解度越大质量分数也就越大,而t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,故所得溶液中溶质质置分数的大小关系是b>a>c.
股答案为:(1)50g;(2)加入c物质(或升高温度、蒸发水);(3)C.
点评 了解溶解度曲线的意义、饱和溶液中溶解度大则溶质的质量分数大、饱和溶液和不饱和溶液之间的相互转化方法即可顺利解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列关于空气成分的说法错误的是( )
| A. | 空气的成分按体积算,氧气约占21% | |
| B. | 稀有气体常用于医疗救急 | |
| C. | 焊接金属时常用氮气作保护气 | |
| D. | 二氧化碳是植物光合作用的重要原料 |
14.下列叙述中,正确的是( )
| A. | 溶液都是无色透明的液体 | |
| B. | 物质的溶解过程通常会伴随着能量的变化 | |
| C. | 配制溶液时,搅拌可以增大固体物质的溶解度 | |
| D. | 60℃时硝酸钾的溶解度为110g,其溶液中溶质与溶剂的质量比为11:21 |
18.为了维持人体的健康生命活动,人体不同器官的体液保持一定的酸碱度范围:
根据上表可知,正常情况下,下列叙述中正确的是( )
| 体液 | 血液 | 唾液 | 胃液 |
| pH | 7.35-7.45 | 6.6-7.2 | 0.9-1.5 |
| A. | 人的血液一定呈碱性 | |
| B. | 人的胃液一定能使紫色石蕊试液变成蓝色 | |
| C. | 人的唾液一定呈酸性 | |
| D. | 用pH试纸能够精确测定以上体液的pH |
6.用同一种基本反应类型,经过两步反应不能实现的转化是( )
| A. | C→H2CO3 | B. | Cu→Cu(OH)2 | C. | H2O2→H2 | D. | NaOH→BaSO4 |