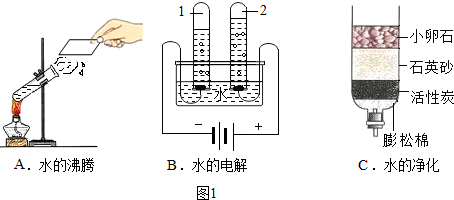
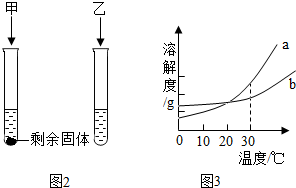
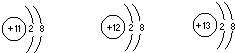题目内容
2.某化学兴趣小组的同学向氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象.【提出问题】氢氧化钠与稀盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下表所示实验方案,请你帮他们完成实验报告.
| 同 学 | 实 验 操作 | 现 象 |
| 甲 | 将稀盐酸慢慢滴入加有酚酞的NaOH溶液,并不断搅拌 | 溶液颜色的变化是红色逐渐变浅直至褪去 |
| 乙 | 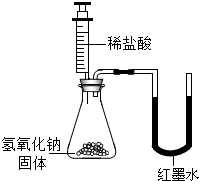 | U型玻璃管中左边的红墨水液面下降(所加稀盐酸的体积忽略不计) |
| 丙 | 用pH试纸测定氢氧化钠溶液的pH, 向其中滴加过量稀盐酸,再测定溶液的pH | 最后溶液的pH≤7(填“>7”“<7”或“=7”) |
【评价反思】你认为实验设计方案不合理的同学是乙,理由是氢氧化钠固体溶于水也会放出热量.
分析 酚酞试液遇到碱溶液变红,遇到中性溶液或酸性溶液不变色,所以氢氧化钠中滴加盐酸使,当把氢氧化钠反应完了,溶液就会变为无色,根据方程式的书写注意事项写出方程式;氢氧化钠固体溶于水会放出大量的热,由于热胀冷缩,所以U型玻璃管中左侧下降右侧上升;测定溶液的pH最简单的方法是使用pH试纸;中性溶液或酸性溶液都不能使酚酞试液变色;由于乙同学用的是氢氧化钠固体溶于水,由于氢氧化钠固体溶于水会放出热量,到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断,所以说法错误.
解答 解:【实验设计】酚酞试液遇到碱溶液变红,遇到中性溶液或酸性溶液不变色,所以氢氧化钠中滴加盐酸使,当把氢氧化钠反应完了,溶液就会变为无色;反应物是氢氧化钠和盐酸,生成物是氯化钠和水,所以方程式是:HCl+NaOH=NaCl+H2O;
氢氧化钠固体溶于水会放出大量的热,氢氧化钠与盐酸反应也能放出热量,会导致瓶内温度升高,由于热胀冷缩,所以U型玻璃管中液面左侧下降右侧上升;
测定溶液的pH最简单的方法是使用pH试纸;中性溶液或酸性溶液都不能使酚酞试液变色所以最后所得溶液的pH值可能小于7,也可能等于7;
【评价反思】由于氢氧化钠固体溶于水会放出热量,到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断,所以乙同学的实验现象不能说明氢氧化钠与盐酸发生了反应;
故答案为:[实验设计]甲:红色逐渐变浅直至褪去;
乙:左;
丙:pH试纸;≤7;
[评价反思]乙;氢氧化钠固体溶于水也会放出热量.
点评 本题是已设计的实验方案进行评价,以及自己设计实验方案的题目,要注意考虑所涉及物质的化学性质,据它们的化学性质来设计方案,这是我们解题的大方向.

练习册系列答案
相关题目
12.下列生活事例中,属于化学变化的是( )
| A. | 把西瓜榨成汁 | B. | 给自行车瘪胎打气 | ||
| C. | 把铁丝弯曲成衣架 | D. | 铁锅生锈 |
10.实验室制取下列物质,选用药品正确的是( )
| A. | 镁和稀硝酸制氢气 | B. | 氧化镁和盐酸制氯化镁 | ||
| C. | 碳酸钙与稀硫酸制二氧化碳 | D. | 铜与硫酸钠反应制取硫酸铜 |
7.下列变化中,属于化学变化的是( )
| A. | 纸张燃烧 | B. | 瓷碗破碎 | C. | 冰块融化 | D. | 铁丝弯曲 |
14.下列典故主要体现化学变化的是( )
| A. | 火烧赤壁 | B. | 铁杵磨成针 | C. | 司马光砸缸 | D. | 凿壁偷光 |
13.如图为制取水煤气(混合气体)的微观示意图,下列说法中正确的是( )

| A. | 该反应中含两种有机化合物 | B. | 水煤气的成分是一氧化碳和氧气 | ||
| C. | 该反应为置换反应 | D. | 该反应中反应物的质量比为8:9 |