题目内容
今年我国“世界环境日”的主题是向污染宣战,某化工厂排放的废水中含有氢氧化钾和碳酸钾.提取50g废水样品于集气瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,共得到硫酸钾98g,同时收集到2.2g二氧化碳,求该废水样品中氢氧化钾的质量.
解:反应消耗的硫酸质量为:98g+2.2g﹣50g=50.2g
设,碳酸钾消耗的硫酸溶液质量为x,
K2CO3+H2SO4=K2SO4+H2O+CO2↑;
98 44
x•10% 2.2g
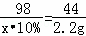 x=49g
x=49g
故氢氧化钾消耗的硫酸溶液质量为:50.2g﹣49g=3.2g
设,废水样品中氢氧化钾的质量为y,
2KOH+H2SO4=K2SO4+2H2O
112 98
y 3.2g×10%
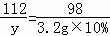 y=0.366g
y=0.366g
答:废水样品中氢氧化钾的质量是0.366g;

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
如表中除去物质所含少量杂质的方法,错误的是()
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 氮气 | 氧气 | 将气体缓缓通过足量的灼热铜网 |
| B | 氧化钙 | 碳酸钙 | 高温煅烧 |
| C | 氯化钙溶液 | 盐酸 | 加过量氢氧化钙溶液 |
| D | 氯化钠溶液 | 氯化镁 | 加过量氢氧化钠溶液,过滤、再向滤液中加适量稀盐酸至溶液pH=7 |
下列事例中,不是通过化学反应提供能量的是( )
|
| A. |
蓄电池放电 | B. |
水力发电 |
|
| C. |
内燃机做功冲程 | D. |
火箭点火升空 |
现有9.3g NaOH与Na2CO3的固体混合物,测得其中钠元素与碳元素的质量比为23:3.在室温下,将该混合物与50g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为57.1g,则原固体混合物中含有钠元素的质量为下列的(C)
|
| A. | 1.15g | B. | 2.3g | C. | 4.6g | D. | 6.9g |





 氧化铜的质量)=________。
氧化铜的质量)=________。 ,需要氧气的质量为________,生成的氧化铜的质量为________。
,需要氧气的质量为________,生成的氧化铜的质量为________。
 H2+CO
H2+CO 2H2↑+O2↑ D.电解水:2H2O
2H2↑+O2↑ D.电解水:2H2O