题目内容
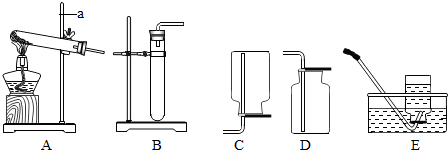
结合下图所示实验装置,回答下列问题:

(1)指出图中标有数字的仪器名称:① ②
(2)实验室用B装置制取氧气时,有关的化学反应方程式 ;若要收集较为纯净的氧气最好选用 .现将85g过氧化氢溶液加入wg二氧化锰反应完全后,留下混合物质量仍为85g,则产生氧气 g.过氧化氢溶液中溶质的质量分数为 .
(3)如果用F装置干燥氧气,则F装置中应装入的液体是 ,氧气应从 端(填“a”或“b”)进入F中;如果用装满水的F装置收集氢气,则氢气应从 端(填“a”或“b”)进入F中.
(4)实验室制取二氧化碳时可用F装置检验二氧化碳.该反应的化学方程式为 .小海用G图装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是 (填序号,可重复选用).
①从b端通氮气
②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳
④从分液漏斗中滴加适量水.

(1)指出图中标有数字的仪器名称:①
(2)实验室用B装置制取氧气时,有关的化学反应方程式
(3)如果用F装置干燥氧气,则F装置中应装入的液体是
(4)实验室制取二氧化碳时可用F装置检验二氧化碳.该反应的化学方程式为
①从b端通氮气
②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳
④从分液漏斗中滴加适量水.
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的检验和验满,有关溶质质量分数的简单计算,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据常见仪器的名称和用途进行解答;
(2)根据B装置适用于固体和液体混合不需要加热的反应,所以可用过氧化氢分解制取氧气,据反应原理书写方程式;氧气不易溶于水,所以可用排水法收集较为纯净的氧气,利用混合物减少的质量就是生成氧气的质量求出过氧化氢的质量,进而求出过氧化氢溶液中溶质的质量分数即可;
(3)根据浓硫酸具有吸水性以及氢气的密度小于水的密度进行解答;
(4)检验二氧化碳用澄清的石灰水,二氧化碳能和水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,据此分析解答.
(2)根据B装置适用于固体和液体混合不需要加热的反应,所以可用过氧化氢分解制取氧气,据反应原理书写方程式;氧气不易溶于水,所以可用排水法收集较为纯净的氧气,利用混合物减少的质量就是生成氧气的质量求出过氧化氢的质量,进而求出过氧化氢溶液中溶质的质量分数即可;
(3)根据浓硫酸具有吸水性以及氢气的密度小于水的密度进行解答;
(4)检验二氧化碳用澄清的石灰水,二氧化碳能和水反应生成碳酸,碳酸显酸性,能使石蕊试液变红色,据此分析解答.
解答:解:(1)图中标有数字的仪器名称分别是:①酒精灯; ②集气瓶;
(2)B装置适用于固体和液体混合不需要加热的反应,所以实验室用B装置制取氧气时,可用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学反应方程式:2H2O2
2H2O+O2↑;收集较为纯净的气体用排水法,氧气不易溶于水,所以可用排水法收集;根据质量守恒定律可知:反应中减少的质量就是氧气的质量,所以生成氧气的质量是wg
设溶液中过氧化氢的质量为x
2H2O2
2H2O+O2↑
68 32
x wg
=
x=
wg
过氧化氢溶液中溶质的质量分数=
×100%=
×100%=2.5w%
(3)浓硫酸具有吸水性,所以用F装置干燥氧气,则F装置中应装入的液体是浓硫酸,氧气应从a进入F中,让气体与浓硫酸充分接触;氢气的密度小于水的密度,所以用装满水的F装置收集氢气,则氢气应从b进入F中;
(4)二氧化碳能和石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是:首先将用石蕊溶液染成紫色的干燥纸花放入广口瓶中,再从a端通二氧化碳,干燥纸花不变色,说明二氧化碳不能使石蕊变色,再从b端通氮气,把二氧化碳排出,再从分液漏斗中滴加适量水,干燥纸花不变色,说明水不能使石蕊变色,再从a端通二氧化碳,纸花变红色,说明二氧化碳和水反应生成了使石蕊变红色的物质--碳酸;
故答案为:(1)酒精灯;集气瓶;
(2)2H2O2
2H2O+O2↑;D;2.5w%;
(3)浓硫酸;a;b;
(4)CO2+Ca(OH)2═CaCO3↓+H2O;②③①④③.
(2)B装置适用于固体和液体混合不需要加热的反应,所以实验室用B装置制取氧气时,可用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学反应方程式:2H2O2
| ||
设溶液中过氧化氢的质量为x
2H2O2
| ||
68 32
x wg
| 68 |
| 32 |
| x |
| wg |
x=
| 68 |
| 32 |
过氧化氢溶液中溶质的质量分数=
| ||
| 85g |
| w |
| 40 |
(3)浓硫酸具有吸水性,所以用F装置干燥氧气,则F装置中应装入的液体是浓硫酸,氧气应从a进入F中,让气体与浓硫酸充分接触;氢气的密度小于水的密度,所以用装满水的F装置收集氢气,则氢气应从b进入F中;
(4)二氧化碳能和石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是:首先将用石蕊溶液染成紫色的干燥纸花放入广口瓶中,再从a端通二氧化碳,干燥纸花不变色,说明二氧化碳不能使石蕊变色,再从b端通氮气,把二氧化碳排出,再从分液漏斗中滴加适量水,干燥纸花不变色,说明水不能使石蕊变色,再从a端通二氧化碳,纸花变红色,说明二氧化碳和水反应生成了使石蕊变红色的物质--碳酸;
故答案为:(1)酒精灯;集气瓶;
(2)2H2O2
| ||
(3)浓硫酸;a;b;
(4)CO2+Ca(OH)2═CaCO3↓+H2O;②③①④③.
点评:该题从实验室制取氧气,以及二氧化碳的性质的实践出发,考查许多可能出现的问题,对于学生掌握制取氧气的方法以及实践活动都有积极的指导意义.

练习册系列答案
相关题目
生活中的下列现象一定属于化学变化的是( )
| A、汽车爆胎 | B、水的蒸馏 |
| C、大米碾碎 | D、燃放鞭炮 |
 化学小组的同学利用如图所示的装置进行实验.回答相关问题:
化学小组的同学利用如图所示的装置进行实验.回答相关问题:
 小明购得用于食用菌种植的轻质碳酸钙,标签如图所示.为测定其含钙量小明进行的实验如下:
小明购得用于食用菌种植的轻质碳酸钙,标签如图所示.为测定其含钙量小明进行的实验如下: