题目内容
4.有100g 10%的食盐溶液,要使其质量分数变为20%,有三种方法,按要求填空:(1)蒸发水分,其质量为50g;
(2)与质量分数大于20%的浓食盐溶液混合,若混入25%的食盐溶液,其溶液质量为200g.
分析 (1)根据溶液在蒸发前后溶质的质量不变来列等式解答;
(2)根据两份溶液在混合时溶质的质量之和等于所得溶液中溶质的质量来解答.
解答 解:(1)设蒸发水的质量为y,
则根据蒸发前后溶质的质量不变得,
100g×10%=(100g-y)×20%
y=50g
(2)设质量分数为25%的溶液为z,
则10%的溶液中的溶质与25%的溶液中的溶质之和等于20%溶液中的溶质,
100g×10%+z×25%=(100g+z)×20%
z=200g
故答案为:(1)50;
(2)200.
点评 本题考查了两种增大溶液质量分数的方法及其计算,学生需要明确不同方法中变化的量和不变的量,明确溶质的关系来解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列物质在水溶液中能大量共存的是( )
| A. | HCl Ca(OH)2 NaNO3 | B. | NaCl K2CO3 H2SO4 | ||
| C. | HCl BaCl2 CuSO4 | D. | KNO3 NaOH Na2CO3 |
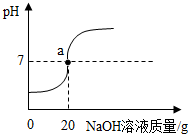 向50g氯化氢和氯化钠的混合溶液中滴加溶质质量分数为20%的氢氧化钠溶液,得到溶液的pH变化曲线如图所示,请回答下列问题:
向50g氯化氢和氯化钠的混合溶液中滴加溶质质量分数为20%的氢氧化钠溶液,得到溶液的pH变化曲线如图所示,请回答下列问题: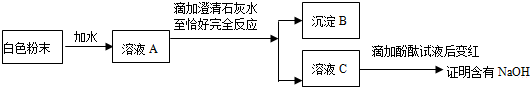
 )与B(
)与B(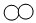 )反应生成C(
)反应生成C(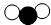 )及反应前后分子及其数目的变化,则该反应的化学方程式中,化学计量数之比为( )
)及反应前后分子及其数目的变化,则该反应的化学方程式中,化学计量数之比为( )
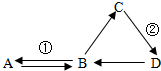 已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如右图所示(部分物质和反应条件已略去).
已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如右图所示(部分物质和反应条件已略去).


