题目内容
5.下列关于燃烧和灭火的说法,不正确的是( )| A. | 将木柴架空燃烧,目的是增大可燃物与氧气的接触面积,促进燃烧 | |
| B. | 逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面逃离 | |
| C. | 救火时,不要贸然打开所有门窗,以兔空气对流促进火势蔓延 | |
| D. | 油锅着火,用锅盖盖上,是为了降低可燃物的温度 |
分析 A、根据促进可燃物燃烧的方法有:增大可燃物与氧气的接触面积或增大氧气的浓度,进行分析判断.
B、根据湿毛巾有类似防毒面具作用、气体受热密度变小,进行分析判断.
C、贸然打开所有门窗,空气流通,使氧气更充足,进行分析判断.
D、根据灭火的原理,进行分析判断.
解答 解:A、将木柴架空燃烧,能增大可燃物与氧气的接触面积,促进燃烧,故选项说法正确.
B、湿毛巾有类似防毒面具作用,用湿毛巾捂住口鼻能防止吸入燃烧时生成的烟尘;气体受热密度变小,有毒气体上升聚集在高处,故要尽量贴近地面逃离,故选项说法正确.
C、救火时,不要贸然打开所有门窗,否则空气流通,使氧气更充足,火势更旺,会导致火势迅速蔓延,不利于灭火,故选项说法正确.
D、油锅着火,用锅盖盖上,利用的是隔绝氧气的灭火原理,故选项说法错误.
故选:D.
点评 本题难度不大,掌握燃烧的条件、灭火的原理、促进可燃物燃烧的方法等并能灵活运用是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.为及时发现燃气泄漏,常在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇在煤气燃烧过程中也发生燃烧,其反应如下:2C2H5SH+9O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+6H2O+2X,下列关于X的说法正确的是( )
| A. | X由碳、硫、氧三种元素组成 | B. | X属于有机化合物 | ||
| C. | X中硫、氧元素的原子个数比为1:2 | D. | X中氧元素的质量分数为60% |
13.下列实验方案不能达到实验目的是( )
| 实验目的 | 实验方案 | |
| A | 验证铝、铜、银三种金属的活动性顺序 | 将洁净的铜丝分别浸入硫酸铝溶液和硝酸银溶液中 |
| B | 用一种试剂一次性鉴别出稀硫酸、澄清石灰水和碳酸钠溶液 | 分别取样,滴加紫色石蕊试液 |
| C | 除去碳粉中混有的少量氧化铜 | 加入足量的稀硫酸,过滤、洗涤、干燥 |
| D | 检验露置的氢氧化钠是否变质 | 取样,加水溶解,滴加氯化钡溶液 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
20.下列说法不正确的是( )
| A. | 空气中N2的体积分数约为78% | |
| B. | O2的化学性质比较活泼,具有可燃性 | |
| C. | CO2是绿色植物光合作用的原料之一 | |
| D. | 稀有气体化学性质稳定,可用作保护气 |
5.物质在“潮湿的空气”中发生变化与空气中某些气体有关.下列说法不正确的是( )
| A. | 钢铁生锈与氧气、水蒸气有关 | |
| B. | 氢氧化钠固体潮解、变质,与水蒸气、二氧化碳有关 | |
| C. | 铜器表面生成铜绿[Cu2(OH)2CO3]与O2、CO2、水蒸气有关 | |
| D. | 生石灰堆放久了变质与氧气有关 |
6. 硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.
硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.
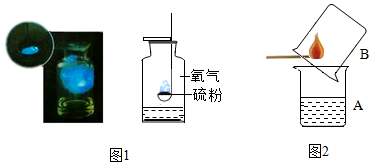
【实验1】在燃烧匙中放入少量硫粉,将燃烧匙放在酒精灯火焰上加热,观察到的现象是发出淡蓝色火焰,产生有刺激性气味的气体,放出热量;然后,将燃烧匙连燃着的硫一起伸入充满氧气的集气瓶中,这时你所能观察到的不同现象是燃烧更剧烈,发出明亮的蓝紫色火焰;上述实验中发生反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
【实验2】
(1)用一支50mL的注射器从充满二氧化硫的集气瓶中抽取40mL二氧化硫,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,观察到的实验现象是溶液变为红色.
(2)将另一支50mL的注射器抽取40mL的空气,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,所观察到的实验现象是无明显现象.
【实验3】如图2所示,先在小烧杯A中加入少量浅紫红色的稀高锰酸钾溶液,再取一根小木条,在一头蘸一些硫粉并点燃,迅速伸入烧杯B中,片刻后立即取出小木条,振荡烧杯A,观察发现高锰酸钾溶液褪色,化学方程式为:2KMnO4+5SO2+2H2O═K2O4+MnSO4+2H2SO4(标出有化合价发生变化的元素的化合价).
此反应用四种基本反应类型无法界定,但因其有元素化合价升降,称之为氧化-还原反应.
 硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.
硫的外观为淡黄色脆性结晶或粉末,俗称硫磺.它有特殊臭味且不溶解于水,微溶于乙醇,易溶于二硫化碳.【实验1】在燃烧匙中放入少量硫粉,将燃烧匙放在酒精灯火焰上加热,观察到的现象是发出淡蓝色火焰,产生有刺激性气味的气体,放出热量;然后,将燃烧匙连燃着的硫一起伸入充满氧气的集气瓶中,这时你所能观察到的不同现象是燃烧更剧烈,发出明亮的蓝紫色火焰;上述实验中发生反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
【实验2】
(1)用一支50mL的注射器从充满二氧化硫的集气瓶中抽取40mL二氧化硫,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,观察到的实验现象是溶液变为红色.
(2)将另一支50mL的注射器抽取40mL的空气,再从小烧杯中抽取10mL滴有紫色石蕊试液的水溶液,用橡皮塞堵住注射器的针孔,慢慢压缩注射器栓塞,所观察到的实验现象是无明显现象.
【实验3】如图2所示,先在小烧杯A中加入少量浅紫红色的稀高锰酸钾溶液,再取一根小木条,在一头蘸一些硫粉并点燃,迅速伸入烧杯B中,片刻后立即取出小木条,振荡烧杯A,观察发现高锰酸钾溶液褪色,化学方程式为:2KMnO4+5SO2+2H2O═K2O4+MnSO4+2H2SO4(标出有化合价发生变化的元素的化合价).
| Mn化合价 | +7 | +6 | +4 | +2 | 0 |
| 化学式 | KMnO4 | K2MnO4 | MnO2 | MnSO4 | Mn |
| 类别 | 盐 | 盐 | 氧化物 | 盐 | 单质 |