题目内容
1. 含有相同离子的盐具有相似的性质.
含有相同离子的盐具有相似的性质.(1)CuCl2、CuSO4的溶液都呈蓝色,是因为它们的溶液中都存在Cu2+(填离子符号).
(2)向CuSO4溶液中加入KOH溶液,充分振荡,反应的化学方程式为CuSO4+2KOH=Cu(OH)2↓+K2SO4.
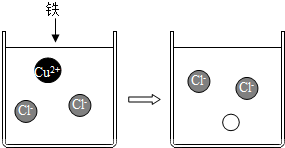
(3)①向CuCl2溶液中加入光亮的铁钉,充分反应后,可观察到的现象是铁钉表面出现红色物质,溶液由蓝色变为浅绿色.如图表示该反应前后溶液中存在的主要离子,请写出如图反应后溶液中“
 ”代表的离子符号Fe2+.
”代表的离子符号Fe2+.②除CuCl2溶液外,将铁钉加入C(选填项)溶液中也能产生相同的实验现象.
A、CuSO4 B、NaCl C、Cu(NO3)2 D、AgNO3.
分析 (1)根据盐的组成写出含有的离子符号;
(2)根据碱和盐生成新碱和新盐写出反应的化学方程式;
(3)①根据在金属活动性顺序中,铁排在铜之前,所以铁会和氯化铜反应生成铜和氯化亚铁进行分析;
②根据反应前后的溶液酸根离子和金属离子的个数比是2:1,然后确定可以代替的物质.
解答 解:(1)CuCl2、CuSO4的溶液都呈蓝色,是因为它们的溶液中都存在Cu2+;
(2)氢氧化钾和硫酸铜反应生成氢氧化铜沉淀和硫酸钾,化学方程式为:CuSO4+2KOH=Cu(OH)2↓+K2SO4;
(3)①在金属活动性顺序中,铁排在铜之前,所以铁会和氯化铜反应生成铜和氯化亚铁,所以可观察到的现象是铁钉表面出现红色物质,溶液由蓝色变为浅绿色,反应后溶液中“ ”代表的离子符号Fe2+;
”代表的离子符号Fe2+;
②反应前后的溶液酸根离子和金属离子的个数比是2:1,除CuCl2溶液外,将铁钉加入Cu(NO3)2 溶液中也能产生相同的实验现象,故选:C.
故答案为:(1)Cu2+;
(2)CuSO4+2KOH=Cu(OH)2↓+K2SO4;
(3)①铁钉表面出现红色物质,溶液由蓝色变为浅绿色,Fe2+;
②C.
点评 在金属活动性顺序中,活动性强的金属能将活动性弱的金属从其盐溶液中置换出来.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
12.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在碳酸钠溶液中:K+、Ca2+、Cl- | |
| B. | 在氢氧化钠溶液中:NH4+、Ca2+、NO3- | |
| C. | 在氯化钾溶液中:Na+、K+、CO32- | |
| D. | 在硫酸钠溶液中:Ba2+、Cl-、OH- |
9. 小化用如图的形式对所学知识进行归纳(其中甲包含乙、丙、丁…),如表中的相应内容中有错误的一组是( )
小化用如图的形式对所学知识进行归纳(其中甲包含乙、丙、丁…),如表中的相应内容中有错误的一组是( )
 小化用如图的形式对所学知识进行归纳(其中甲包含乙、丙、丁…),如表中的相应内容中有错误的一组是( )
小化用如图的形式对所学知识进行归纳(其中甲包含乙、丙、丁…),如表中的相应内容中有错误的一组是( )| 甲 | 乙、丙、丁… | |
| A | 溶液 | 碘酒、糖水、生理盐水… |
| B | 合金 | 不锈钢、焊锡、生铁… |
| C | 干燥剂 | 石灰石、浓硫酸、生石灰… |
| D | 无机化合物 | 酸、碱、盐、氧化物… |
| A. | A | B. | B | C. | C | D. | D |
16. 为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符合,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表:
为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符合,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表:
(1)反应共生成BaSO4的质量为23.3g.反应前后,溶液中氯元素的质量是不变(填“不变”、“增大”或“减小”).
(2)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符.(请写出计算过程)
 为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符合,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表:
为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符合,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表:| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量/g | 氯化钡溶液质量/g | 过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
(2)若所取氮肥样品的质量为15g,试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符.(请写出计算过程)
6.下列实验现象描述正确的是( )
| A. | 红磷在空气中燃烧产生大量白雾 | |
| B. | 铁丝在空气中燃烧时,火星四射,生成黑色固体 | |
| C. | 木炭在氧气中燃烧发出白光,生成黑色固体 | |
| D. | 氢气在空气中燃烧,发出淡蓝色火焰 |
11.下列归纳和总结完全正确的一组是( )
| A.知识经验 | B.前者属物理性质,后者属化学性质 |
| ①不锈钢属于复合材料 ②二氧化碳和一氧化碳中碳元素化合价不同 ③煤气泄漏立即打开油烟机排气 | ①浓盐酸的挥发性,活性炭的吸附性 ②甲烷的可燃性氧气的助燃性 ③一氧化碳的还原性 金属的导电性 |
| C.解释或者结论 | D.可做的家庭实验 |
| ①“花香四溢”-分子在不断运动 ②溶液中加酚酞不变色-溶液的PH=7 ③水通电分解-在化学变化中,分子可以再分 | ①用蒸馏法使硬水转化成软水 ②用鸡蛋壳和食醋制二氧化碳 ③用月季花和酒精自制酸碱指示剂 |
| A. | A | B. | B | C. | C | D. | D |
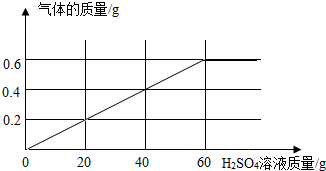 某铁矿粉,主要成分为铁的氧化物(FexOy),一学生利用实验作进一步分析,过程及数据如下.(注:铁矿粉中杂质不参与下列过程中的反应)
某铁矿粉,主要成分为铁的氧化物(FexOy),一学生利用实验作进一步分析,过程及数据如下.(注:铁矿粉中杂质不参与下列过程中的反应)