题目内容
6.对“10%的食盐溶液”含义的解释正确的是( )| A. | 100 g水中溶解了10 g食盐 | |
| B. | 100 g食盐溶液中溶解了10 g食盐 | |
| C. | 将10 g食盐溶解于90 g水中所得的溶液 | |
| D. | 将食盐、食盐水按1:10的质量比配成的溶液 |
分析 溶质的质量分数是指溶质质量与溶液质量之比,其含义是指100份质量的某溶液中含多少份质量的该溶质.
解答 解:溶质质量分数为10%的食盐溶液即溶液中溶质和溶液的质量之比是10:100,或溶质和溶剂的质量之比为10:90.
A、10%的食盐溶液是指100g食盐溶液中溶解了10g食盐,而不是100g水中溶解了10g食盐,故A解释错误;
B、由A的分析可知:100g食盐溶液中溶解有10g食盐解释正确,故B解释正确;
C、将10g食盐溶解在90g水中所得的溶液,溶质和溶液的质量比是10g:100g,即10:100,故C解释正确;
D、10%的食盐溶液中食盐与水的质量比是10:90,不是1;10,故D解释错误.
故选BC.
点评 本题难度不大,主要考查了对溶液中溶质的质量分数的理解和应用.

练习册系列答案
相关题目
17.某同学为了探究酸和碱的反应,按下列要求进行了实验的设计与分析:
【实验目的】证明酸和碱发生了中和反应.
【演示实验】将一定量的稀硫酸加入到盛有NaOH溶液的小烧杯中.
【实验原理】该反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,该同学产生了疑问:反应后溶液中的溶质是什么呢?
【实验探究】该同学又选取了BaCl2、酚酞、紫色石蕊溶液设计实验,分别探究上述酸、碱反应后烧杯中溶液中的溶质,取烧杯中溶液,按下列方案进行实验:
①设计的三个方案中,有一个错误的方案是:方案一,该方案错误的原因是即使稀硫酸不过量,也会出现白色沉淀,因为溶液中有生成的硫酸钠,存在硫酸根离子;
②请你简单设计实验对上述错误方案进行更正:取样,滴入几滴紫色石蕊溶液,液变红,溶液呈酸性,说明硫酸过量.
【实验目的】证明酸和碱发生了中和反应.
【演示实验】将一定量的稀硫酸加入到盛有NaOH溶液的小烧杯中.
【实验原理】该反应的化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,该同学产生了疑问:反应后溶液中的溶质是什么呢?
【实验探究】该同学又选取了BaCl2、酚酞、紫色石蕊溶液设计实验,分别探究上述酸、碱反应后烧杯中溶液中的溶质,取烧杯中溶液,按下列方案进行实验:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液颜色为紫色 | 酸碱恰好完全反应 |
| 方案三 | 取样,滴入几滴无色酚酞溶液 | 溶液变红 | 氢氧化钠过量,溶质为氢氧化钠和硫酸钠 |
②请你简单设计实验对上述错误方案进行更正:取样,滴入几滴紫色石蕊溶液,液变红,溶液呈酸性,说明硫酸过量.
1.下列物质的化学式、俗名与分类均正确的是( )
| A. | Na2CO3 纯碱 碱 | B. | CaO 生石灰 氧化物 | ||
| C. | O2 臭氧 单质 | D. | NaHCO3 苏打 盐 |
11.空气的成分中能供给人体呼吸的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 稀有气体 | D. | 二氧化碳 |
15.2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青嵩素(化学式C15H22O5),是一种治疗疟疾的特效药,下列说法正确的是( )
| A. | 青嵩素属于氧化物 | |
| B. | 青嵩素的相对分子质量是282g | |
| C. | 青嵩素由42个原子构成 | |
| D. | 青嵩素中碳、氢元素的质量比为90:11 |
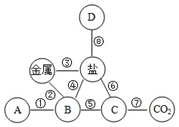 如图是小李同学构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.请按要求回答下列问题:
如图是小李同学构建的知识网络,其中A、B、C、D分别表示不同类别的化合物,“-”表示物质之间能够发生化学反应.请按要求回答下列问题: