题目内容
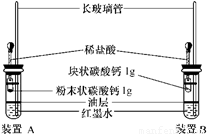
小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时捏扁两滴管的胶头,并观察实验现象.(1)你估计两根玻璃导管中的实验现象是______;
(2)小明的实验目的是:______.

【答案】分析:(1)根据碳酸钙可以和盐酸反应生成气体,同时接触面积越大,反应速率越快,据此分析解答玻璃导管中的实验现象.
(2)根据图示分析可知:同浓度同体积的稀盐酸与块状和粉末状的碳酸钙反应,是为了验证反应物的接触面积对反应速率的影响.
解答:解:(1)粉末状的碳酸钙与块状的碳酸钙均能与盐酸反应产生气体,粉末状的碳酸钙与盐酸的接触面积大,反应速率比块状的碳酸钙快,相同时间产生气体多,所以装置A中导管内液面的上升速度比装置B的快.
(2)分析装置A和装置B可知:同浓度同体积的稀盐酸与块状和粉末状的碳酸钙反应,即只有碳酸钙形状不同,则可推知实验目的是比较粉末状和块状碳酸钙和同浓度、同体积盐酸反应的速率.
故答案为:(1)两装置中导管内的液面均上升,装置A中导管内液面的上升速度比装置B中的快;
(2)比较粉末状和块状的碳酸钙和同浓度、同体积盐酸反应速率的大小.
点评:本题难度不是很大,控制变量法是实验探究常采用的方法,本题通过控制盐酸的浓度和质量都相等的条件下验证颗粒大小与反应速度的关系.
(2)根据图示分析可知:同浓度同体积的稀盐酸与块状和粉末状的碳酸钙反应,是为了验证反应物的接触面积对反应速率的影响.
解答:解:(1)粉末状的碳酸钙与块状的碳酸钙均能与盐酸反应产生气体,粉末状的碳酸钙与盐酸的接触面积大,反应速率比块状的碳酸钙快,相同时间产生气体多,所以装置A中导管内液面的上升速度比装置B的快.
(2)分析装置A和装置B可知:同浓度同体积的稀盐酸与块状和粉末状的碳酸钙反应,即只有碳酸钙形状不同,则可推知实验目的是比较粉末状和块状碳酸钙和同浓度、同体积盐酸反应的速率.
故答案为:(1)两装置中导管内的液面均上升,装置A中导管内液面的上升速度比装置B中的快;
(2)比较粉末状和块状的碳酸钙和同浓度、同体积盐酸反应速率的大小.
点评:本题难度不是很大,控制变量法是实验探究常采用的方法,本题通过控制盐酸的浓度和质量都相等的条件下验证颗粒大小与反应速度的关系.

练习册系列答案
相关题目
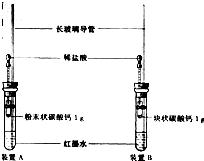 28、小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时完全捏扁两滴管的胶头,并观察实验现象.
28、小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时完全捏扁两滴管的胶头,并观察实验现象.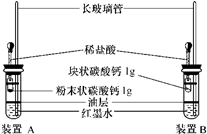 小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时完全捏扁两滴管的胶头,并观察实验现象.
小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时完全捏扁两滴管的胶头,并观察实验现象.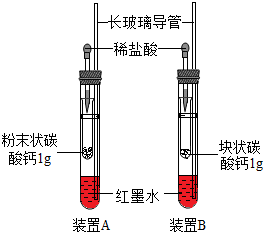 小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时捏扁两滴管的胶头,并观察实验现象.
小明按如图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,同时捏扁两滴管的胶头,并观察实验现象.