题目内容
4.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生反应,一段时间后,测得有关数据如表,则关于此反应认识不正确的是( )| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 3 | 2 | 20 |
| 反应后质量/g | X | 28 | 2 | 0 |
| A. | 该反应的基本类型为化合反应 | |
| B. | 反应后甲物质的质量值x=15 | |
| C. | 物质丙可能是该反应的催化剂 | |
| D. | 参加反应的丁物质与生成的乙物质的质量比为4:7 |
分析 根据质量守恒定律计算出“X”的值,再根据化学反应后,质量增加的物质是生成物,质量减少的物质是反应物结合表中数据进行分析.
解答 解:根据质量守恒定律,反应前后物质的总质量不变,所以20+3+2+20=X+28+2+0,因此X=15g;甲、丁质量都减少,是反应物;乙增加,是生成物;甲反应掉了20g-15g=5g,丁的反应质量为20g-0g=20g,生成的乙的质量为28g-3g=25g.数据可以如下处理:
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 20 | 3 | 2 | 20 |
| 反应后质量(g) | X=15 | 28 | 2 | 0 |
| 质量变化 | -5 | +25 | 0 | -20 |
B、反应后甲物质的质量值x=15,故正确;
C、物质丙的质量在反应前后不变,可能是该反应的催化剂,也可能没有参加反应,故说法正确;
D、参加反应的丁物质与生成的乙物质的质量比为20g:25g=4:5≠4:7,故说法错误.
故选D.
点评 在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
14.下列实验基本操作的叙述正确的是( )
| A. | 用滴管滴加液体时,将滴管伸入试管中 | |
| B. | 用量筒量取7mL液体时,最好选用10mL量筒 | |
| C. | 检验一集气瓶中是否集满氧气,可以将带火星的木条伸入集气瓶中 | |
| D. | 给试管里的液体加热时,试管底部要与酒精灯芯接触 |
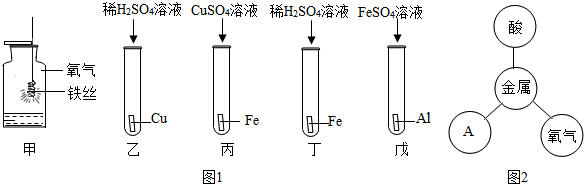
9.通过下列实验,可以得出的相应结论正确的是( )
| A. | 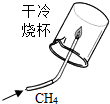 既说明甲烷具有可燃性,又说明甲烷是由氢元素和碳元素组成 | |
| B. |  既说明二氧化碳的密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 | |
| C. | 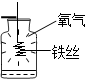 既说明铁丝具有可燃性,又说明增大氧气的浓度能促进燃烧 | |
| D. |  既说明二氧化碳可溶于水,又说明二氧化碳能与水反应 |
16.对于含有68g过氧化氢的双氧水能产生多少克氧气,小海同学利用化学式进行了解答,如表中所示.请改正小海的错误:
改正:设生成氧气的质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
68g x
$\frac{68}{68g}=\frac{32}{x}$,
x=32g,
答:68g过氧化氢的双氧水能产生32g氧气..
| 解:68g过氧化氢中氧元素的质量为:68g×$\frac{20}{{H}_{2}{O}_{2}}$×100%=68g×$\frac{32}{34}$=64g,因为 氧气中的氧元素来自于过氧化氢,所以68g过氧化氢产生氧气的质量为64g. |
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
68g x
$\frac{68}{68g}=\frac{32}{x}$,
x=32g,
答:68g过氧化氢的双氧水能产生32g氧气..