题目内容
2.维生素C的化学式为C6H8O6,下列关于维生素C的叙述正确的是( )| A. | 维生素C是氧化物 | |
| B. | 维生素C由6个碳原子、8个氢原子、6个氧原子构成的 | |
| C. | 维生素C的相对分子质量为l76g? | |
| D. | 维生素C中氧元素质量分数最大 |
分析 A.氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B.根据物质的结构来分析.
C.根据相对分子质量的单位来分析.
D.根据化合物中元素的质量比来分析.
解答 解:A.维生素C是由碳、氢、氧三种元素组成的化合物,不属于氧化物,故选项说法错误.
B.维生素C是由分子构成的,不是由原子直接构成的,故选项说法错误.
C.相对分子质量的单位不是“g”而是“1”,通常省略不写,故选项说法错误.
D.维生素C中碳、氢、氧三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12;可见其中氧元素的质量分数最大,故选项说法正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
12.化学课上教师演示了加热炭粉(过量)和氧化铜混合物的实验,课后课外活动小组同学对教师演示中获得的灰红色粉末样品进行实验.实验装置如图所示(图中铁架台等装置已略去,D中盛放的是固体氢氧化钠和氧化钙的混合物).
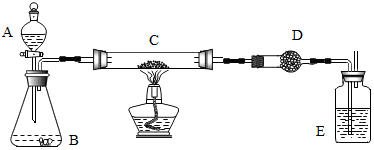
实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g.样品中铜的质量分数=$\frac{[w-(b-a)×\frac{12}{44}]}{w}$
请回答下列问题.
①主要实验内容
②实验讨论
装置E中盛放的试剂是澄清石灰水,其作用是检验D装置是否完全吸收了二氧化碳.
按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),原因是水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大,如果要得到了较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.

实验主要原理:称取样品粉末W g,放入C中;D中装入ag药品;反应结束,冷却后,称量D中药品质量为b g.样品中铜的质量分数=$\frac{[w-(b-a)×\frac{12}{44}]}{w}$
请回答下列问题.
①主要实验内容
| 实验主要步骤 | 实验现象 | 有关化学方程式 |
| 打开A的上塞、活塞,慢慢滴加溶液 | B、E中有气泡 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| 对C进行加热,当C中药品充分反应后,关闭A的活塞,停止加热 | C中的灰红色粉末变成黑色 | C+O2$\frac{\underline{\;点燃\;}}{\;}$ CO2 2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO |
装置E中盛放的试剂是澄清石灰水,其作用是检验D装置是否完全吸收了二氧化碳.
按上述实验,得到铜的质量分数不精确,你认为是偏小(填:偏大、偏小、或不能确定),原因是水蒸气通过C被D中碱石灰吸收,测得二氧化碳质量偏大,如果要得到了较正确的结果,对该装置改进的方法是在装置B与C之间接一个与D相同的装置.
13.下列有关空气的说法正确的是( )
| A. | 空气是一种非常重要的天然资源 | |
| B. | 空气中含量最多的是氧气 | |
| C. | 食物较长时间露置在空气中就会变质,这主要是由于空气中含有氮气 | |
| D. | 若大量有害物质进入空气中,仅靠大自然的自净能力,大气仍能保持洁净 |
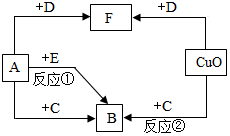 A、B、C、D、E是初中化学中常见的五种无色气体.它们之间的转化关系如图所示.
A、B、C、D、E是初中化学中常见的五种无色气体.它们之间的转化关系如图所示.