题目内容
13.下列对实验现象或事实的分析合理的是( )| A. | 测得某溶液的pH>7,说明该溶液一定呈碱性 | |
| B. | 某无色气体混入空气后点燃爆炸,说明该气体一定是氢气 | |
| C. | 向某固体中加入稀盐酸有气泡产生,说明该物质中一定含有${CO}_{3}^{2-}$ | |
| D. | 某物质在空气中燃烧生成CO2和H2O,说明该物质一定含碳、氢、氧三种元素 |
分析 A、根据溶液的pH与酸碱性的关系进行分析判断;
B、根据可燃性气体的性质考虑;
C、碳酸盐、活泼金属分别与稀盐酸反应放出二氧化碳与氢气,可以据此判断
D、根据质量守恒定律考虑;
解答 解:A、碱性溶液的pH>7,测定某溶液的pH>7,则该溶液一定呈碱性,故正确;
B、可燃性气体的性质:点燃它们与空气或氧气的混合物易发生爆炸,所以某无色气体混入空气后点燃爆炸,不能证明该气体一定是H2还可能是一氧化碳、甲烷等,故错误;
C、活泼金属也可与盐酸反应放出气体氢气,因此向某固体中加入稀盐酸有气泡产生,在未证明气体为二氧化碳时,不能证明该物质中一定含有CO32-故错误;
D、物质在空气中燃烧生成二氧化碳和水,可证明该物质一定含碳、氢两种元素 可能含有氧元素.故错误;
故选:A.
点评 本题难度不大,掌握溶液的酸碱性与pH关系、常见的可燃性物质、酸的性质以及根据质量守恒定律判断物质中元素组成等是正确解答本题的关键.

练习册系列答案
相关题目
4.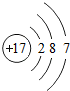 如图是某种元素的结构示意图,下列说法错误的是( )
如图是某种元素的结构示意图,下列说法错误的是( )
 如图是某种元素的结构示意图,下列说法错误的是( )
如图是某种元素的结构示意图,下列说法错误的是( )| A. | 该元素属于非金属元素 | |
| B. | 该原子在化学变化中容易失去电子形成阳离子 | |
| C. | 该原子核外有三个电子层 | |
| D. | 该原子的原子核内有17个质子 |
1. 在学习金属与盐溶液的置换反应时,化学兴趣小组的同学设计了金属钠硫酸铜溶液反应的实验,实验中发现有无色无味的气体产生,同时得到了蓝色的沉淀物,小组同学对生成物的成分进行探究.
在学习金属与盐溶液的置换反应时,化学兴趣小组的同学设计了金属钠硫酸铜溶液反应的实验,实验中发现有无色无味的气体产生,同时得到了蓝色的沉淀物,小组同学对生成物的成分进行探究.
【提出问题】产生的气体是什么?
【猜想与假设】(1)氧气;(2)二氧化硫;(3)氢气.
你认为不合理的猜想是(2),理由是二氧化硫是刺激性气味的气体.
【实验方案】实验小组同学利用如图实验装置进行实验.实验时将生成的气体通过灼热的氧化铜固体,若出现
黑色氧化铜变成红色的现象,就证明生成的气体是氢气.
【查阅资料】钠与冷水能发生剧烈反应,化学方程式为2Na+2H2O═2NaOH+H2↑.
【分析与结论】产生的气体是H2.
探究二:沉淀物的成分是什么?
【进一步猜想】小组同学认为认为沉淀可能是氢氧化钠与硫酸铜反应生成的氢氧化铜;还可能是含有钠直接与硫酸铜反应生成红色的单只铜,知识蓝色的氢氧化铜沉淀掩盖了红色的铜.
【实验方案】请设计实验探究沉淀物的成分,并完成下列实验报告.
实验中反生反应的化学方程式是2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
 在学习金属与盐溶液的置换反应时,化学兴趣小组的同学设计了金属钠硫酸铜溶液反应的实验,实验中发现有无色无味的气体产生,同时得到了蓝色的沉淀物,小组同学对生成物的成分进行探究.
在学习金属与盐溶液的置换反应时,化学兴趣小组的同学设计了金属钠硫酸铜溶液反应的实验,实验中发现有无色无味的气体产生,同时得到了蓝色的沉淀物,小组同学对生成物的成分进行探究.【提出问题】产生的气体是什么?
【猜想与假设】(1)氧气;(2)二氧化硫;(3)氢气.
你认为不合理的猜想是(2),理由是二氧化硫是刺激性气味的气体.
【实验方案】实验小组同学利用如图实验装置进行实验.实验时将生成的气体通过灼热的氧化铜固体,若出现
黑色氧化铜变成红色的现象,就证明生成的气体是氢气.
【查阅资料】钠与冷水能发生剧烈反应,化学方程式为2Na+2H2O═2NaOH+H2↑.
【分析与结论】产生的气体是H2.
探究二:沉淀物的成分是什么?
【进一步猜想】小组同学认为认为沉淀可能是氢氧化钠与硫酸铜反应生成的氢氧化铜;还可能是含有钠直接与硫酸铜反应生成红色的单只铜,知识蓝色的氢氧化铜沉淀掩盖了红色的铜.
【实验方案】请设计实验探究沉淀物的成分,并完成下列实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取蓝色的氢氧化铜固体放入试管中; (2)向试管中滴加稀硫酸溶液 | 蓝色固体溶解消失,变成蓝色溶液,无红色沉淀物 | 该蓝色沉淀中不含不含单质铜 |
18.建立宏观和微观的联系是化学独特的思维方式,下列说法正确的是( )
| A. | 空气是由空气分子构成的 | |
| B. | 金刚石和石墨物理性质差异大的原因是构成它们的碳原子排列方式不同 | |
| C. | 组成水和过氧化氢的元素种类相同,所以它们的化学性质相同 | |
| D. | 分子由原子构成,故分子一定比子原子大 |
5.下列过程中不发生化学变化的是( )
| A. | 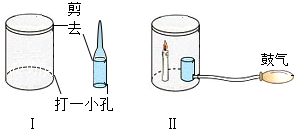 面粉爆炸实验 | B. | 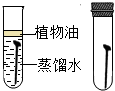 探究铁生锈实验 | ||
| C. |  炉具清洗剂去污 | D. |  面包发霉 |
2.下列实验操作能达到实验目的是( )
| A. | 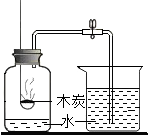 测定空气中氧气含量 | |
| B. | 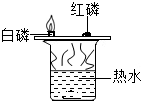 探究燃烧条件之一是氧气 | |
| C. |  过氧化氢溶液与二氧化锰混合制氧气 | |
| D. |  证明分子在不停运动 |
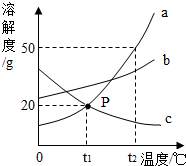 如图是a、b、c三种物质的溶解度曲线,请根据该图回答下列问题:
如图是a、b、c三种物质的溶解度曲线,请根据该图回答下列问题: