题目内容
5.某研究性学习小组欲利用如图装置进行相关气体制取的探究,请你参与分析并回答相关问题.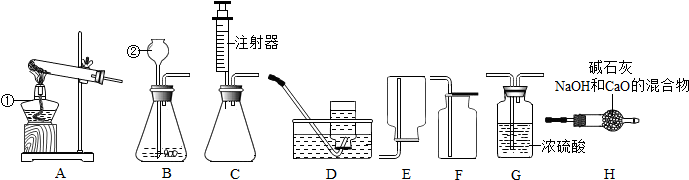
(1)写出图中有标号仪器的名称:①酒精灯、②长颈漏斗;
(2)用双氧水和二氧化锰来制取氧气时,可选用的最佳装置组合是CD或CF(填序号);
(3)实验用氯酸钾制取氧气时,发生反应的化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为如图中最适合制取乙炔气体的发生装置是C(填序号);
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水,其水溶液呈碱性;氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.
①制取并收集一瓶干燥氨气的装置连接顺序为AHE(填序号);
②氨气在加热条件下与氧化铜反应的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑;
③小芳将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是:水进入集气瓶中一部分,溶液由无色变成红色.
分析 (1)认识常见仪器的名称;
(2)反应装置要根据反应物的状态和反应条件决定;根据氧气的性质来确定收集方法;
(3)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
(4)根据注射器可以控制液体的滴加速度进行分析;
(5))①根据实验室常用氯化铵固体与碱石灰固体共热来制取氨气,氨气密度比空气小,极易溶于水进行分析;
②根据氨气和氧化铜在加热的条件下生成铜、氮气和水进行分析;
③根据氨气易溶于水,氨水显碱性,能使酚酞变红色进行分析.
解答 解:(1)①是酒精灯,②是长颈漏斗;故填:酒精灯;长颈漏斗;
(2)双氧水和二氧化锰来制取氧气是固体与液体混合不需要加热制取气体,为了便于控制反应的速率,可选用C装置来制取,氧气的密度比空气大,可用向上排空气法来收集,不易溶于水,可用排水法来收集;故填:CD或CF;
(3)实验室用氯酸钾制取氧气的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
(4)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应加热引起发生装置炸裂.能控制反应速率的为C装置;故填:C;
(5)①实验室常用氯化铵固体与碱石灰固体共热来制取氨气,氨气密度比空气小,极易溶于水,所以制取并收集一瓶干燥氨气的装置连接顺序为:AHE;
②氨气和氧化铜在加热的条件下生成铜、氮气和水,化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑;
③氨气易溶于水,氨水显碱性,能使酚酞变红色,所以观察到的现象是:水进入集气瓶中一部分,溶液由无色变成红色.
故填:①AHE;②2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑;③水进入集气瓶中一部分,溶液由无色变成红色.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

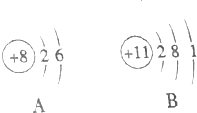 了解物质构成的微观奥秘,能帮助我们更好地认识物质及其变化的本质.
了解物质构成的微观奥秘,能帮助我们更好地认识物质及其变化的本质.(1)氧和碳是人体中含量最多的两种元素,它们的本质区别是质子数不同.
(2)如图所示原子结构示意图中,表示的是金属元素的原子的是B.
| A. | NaClO4 | B. | Cl2 | C. | NaClO | D. | HCl |
| A. | 变大 变小 | B. | 变小 变小 | C. | 变小 变大 | D. | 变大 变大 |
