题目内容
建立宏观、微观和符号之间的联系有重要意义.
(1)下图物质是由不同粒子构成的,请用化学符号表示出构成这些物质的粒子.
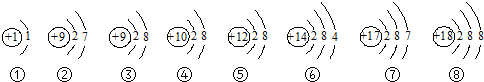
(2)如图所示为某些元素和原子结构的部分信息.

甲图所示元素的元素符号是 ,乙图所示元素的原子的核电荷数是 ,丙图所示的粒子属于 (填“原子”、“阳离子”或“阴离子”).
(3)N(NO2)3是科学家2011年发现的一种新型火箭燃料.试计算N(NO2)3中氮元素和氧元素的质量比为 (结果用最简整数比表示),N(NO2)3中氮元素的质量分数为 (最终结果保留一位小数).
(1)下图物质是由不同粒子构成的,请用化学符号表示出构成这些物质的粒子.
 生命之源-水 |  新型金属材料 纳米铜 |  食盐的主要成分氯化钠 |
| 构成的粒子是 | 构成的粒子是 | 构成的粒子是 |

甲图所示元素的元素符号是
(3)N(NO2)3是科学家2011年发现的一种新型火箭燃料.试计算N(NO2)3中氮元素和氧元素的质量比为
考点:分子、原子、离子、元素与物质之间的关系,原子结构示意图与离子结构示意图,元素周期表的特点及其应用,元素质量比的计算,元素的质量分数计算
专题:化学式的计算,物质的微观构成与物质的宏观组成,化学用语和质量守恒定律
分析:(1)根据金属、大多数固态非金属单质、稀有气体单质等由原子构成,有些物质是由分子构成的,如水、氢气等,有些物质是由离子构成的,如氯化钠,进行分析解答即可.
(2)根据元素周期表提供的信息,原子序数=核外电子数=质子数,元素符号、元素名称,进行解答;
根据当核电荷数=质子数>核外电子数,为阳离子;进行判断;
(3)依据元素的质量比等于各元素相对原子质量和的比分析解答即可;
根据化合物中元素的质量分数
×100%,进行分析判断.
(2)根据元素周期表提供的信息,原子序数=核外电子数=质子数,元素符号、元素名称,进行解答;
根据当核电荷数=质子数>核外电子数,为阳离子;进行判断;
(3)依据元素的质量比等于各元素相对原子质量和的比分析解答即可;
根据化合物中元素的质量分数
| 相对原子质量×原子个数 |
| 相对分子质量 |
解答:解:(1)水是由水分子构成的;铜属于金属单质,是由铜原子直接构成的;氯化钠是由钠离子和氯离子构成的.
(2)根据元素周期表提供的信息,可知甲图中①代表的元素符号是 Al,乙图中所示元素原子的核电荷数是 8;
由微粒结构示意图可知丙图粒子:核电荷数=质子数=12>核外电子数10,为阳离子;
(3)依据元素的质量比等于各元素相对原子质量和的比,所以N(NO2)3中氮元素和氧元素的质量比是14×4:16×6=7:12;
N(NO2)3中氮元素的质量分数为
×100%≈36.8%.
故答案为:(1)H2O; Cu; Na+、Cl-
(2)Al; 8; 阳离子
(3)7:12; 36.8%.
(2)根据元素周期表提供的信息,可知甲图中①代表的元素符号是 Al,乙图中所示元素原子的核电荷数是 8;
由微粒结构示意图可知丙图粒子:核电荷数=质子数=12>核外电子数10,为阳离子;
(3)依据元素的质量比等于各元素相对原子质量和的比,所以N(NO2)3中氮元素和氧元素的质量比是14×4:16×6=7:12;
N(NO2)3中氮元素的质量分数为
| 14×4 |
| 14×4+16×6 |
故答案为:(1)H2O; Cu; Na+、Cl-
(2)Al; 8; 阳离子
(3)7:12; 36.8%.
点评:本题难度不大,掌握物质的微观构成、灵活运用化学式的含义、有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
下列反应属于置换反应的是( )
A、3CO+Fe2O3
| ||||
| B、2Al+3CuSO4═Al2(SO4)3+3Cu | ||||
C、2CO+O2
| ||||
| D、CO2+2NaOH═Na2CO3+H2O |
下列化学方程式书写正确的是( )
| A、Mg+02═MgO2 | ||||
| B、Cu2(OH)2CO3═CuO+H2O+CO2↑ | ||||
| C、H2O2═H2+O2 | ||||
D、CaCO3
|
从环境保护的角度考虑,下列燃料中最理想的是( )
| A、氢气 | B、煤气 | C、酒精 | D、汽油 |
下列家庭常用的调味品中,可视为纯净物的是( )
| A、加碘食盐 | B、食醋 |
| C、白酒 | D、白糖 |