题目内容
15.向某无色溶液中滴加稀硝酸,无现象产生,再滴加BaCl2溶液,若产生白色沉淀,则原溶液中含SO42-.滴加稀硝酸的作用是酸化溶液,防止其他离子的干扰.分析 根据常见酸和盐的物理性质和化学性质即可作答;氯化银、硫酸钡均是不溶于稀硝酸的白色沉淀.
解答 解:氯化钡会电离出Cl-和Ba2+,若向其中加入含SO42-的溶液,会产生不溶于稀硝酸的硫酸钡白色沉淀;
故填:BaCl2;酸化溶液,防止其他离子的干扰.
点评 检验硫酸根的方法是:先将溶液酸化,若无白色沉淀生成,再加氯化钡溶液,若有白色沉淀生成,则证明有硫酸根.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列物质不能由金属和酸反应直接制得的是( )
| A. | ZnCl2 | B. | FeCl3 | C. | MgCl2 | D. | AlCl3 |
3.如图为氮元素在元素周期表中的信息及原子结构示意图.下列有关说法不正确的是( )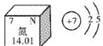

| A. | 氮元素属于非金属元素 | B. | 氮原子核外有2个电子层 | ||
| C. | 氮元素内质子数为7 | D. | 氮元素的相对原子质量是14.01g |
4.分类是学习化学的方法之一,下列物质是按单质、碱、氧化物的顺序排列的是( )
| A. | 氢气、硫酸钠、水 | B. | 氧气、碳酸钙、空气 | ||
| C. | 甲烷、食盐、石油 | D. | 金刚石、熟石灰、冰水 |
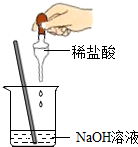 酸与碱作用生成盐和水的反应叫做中和反应,探究中和反应是否发生或酸和碱是否恰好完全反应的方法有多种.某学习小组的同学从不同角度进行有关中和反应的实验探究:
酸与碱作用生成盐和水的反应叫做中和反应,探究中和反应是否发生或酸和碱是否恰好完全反应的方法有多种.某学习小组的同学从不同角度进行有关中和反应的实验探究: