题目内容
(1)质量相等的SO2和SO3中所含氧元素的质量比为 .
(2)有碳化钙(CaC)和碳酸钙(CaCO3)的混合物中,氧元素的质量占20%,则其中钙元素的质量占 .
【考点】化合物中某元素的质量计算;元素的质量分数计算.
【专题】有关化学式的计算.
【分析】(1)根据化合物中某元素的质量=该化合物的质量×该化合物中该元素的质量分数进行分析;
(2)根据在碳化钙(CaC)和碳酸钙(CaCO3)的混合物中,氧元素的质量占20%,所以钙元素、碳元素的质量分数是:1﹣20%=80%,然后依据碳元素和钙元素的相对原子质量进行计算.
【解答】解:(1)设相同质量的二氧化硫和三氧化硫的质量为m,
则所含氧元素的质量比为(m×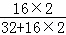 ×100%):(m×
×100%):(m×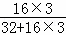 ×100%)=5:6;
×100%)=5:6;
(2)在碳化钙(CaC)和碳酸钙(CaCO3)的混合物中,氧元素的质量占20%,所以钙元素、碳元素的质量分数是:1﹣20%=80%,所以钙元素的质量分数为:80%×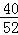 ×100%=62%.
×100%=62%.
故答案为:(1)5:6;
(2)62%.
【点评】本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
以下是空气污染指数与质量级别、质量状况的对应关系:
| 污染指数 | 50以下 | 51~100 | 101~150 | 151~200 | 201~250 | 251~300 | 301以上 |
| 质量级别 | Ⅰ | Ⅱ | Ⅲ(1) | Ⅲ(2) | Ⅳ(1) | Ⅳ(2) | Ⅴ |
| 质量状况 | 优 | 良 | 轻微 污染 | 轻度 污染 | 中度 污染 | 中度 重污染 | 重度 污染 |
赣州市10月某天的空气污染指数为48,首要污染物为可吸入颗粒物。根据以上信息,判断我市当天的空气质量级别和空气质量状况分别是( )
A.Ⅰ 优 B.Ⅱ 良 C.Ⅲ(2)轻度污染 D.Ⅴ 重度污染