题目内容
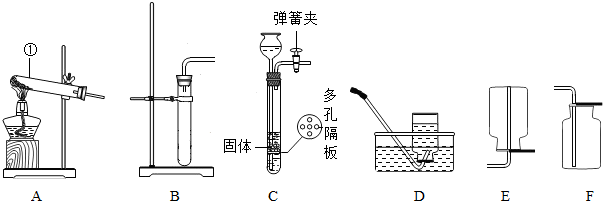
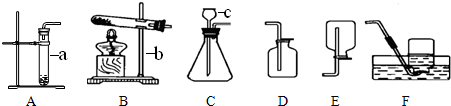
实验室用过氧化氢溶液与二氧化锰混合制氧气.现将1.0g二氧化锰放入盛有20.0g过氧化氢溶液的锥形瓶中,反应结束后,称得锥形瓶中剩余物质的质量为20.2g.计算:
(1)反应结束后,过滤,滤渣的质量为 g.
(2)反应产生氧气的质量为 g.
(3)过氧化氢溶液中溶质的质量分数.
| 根据化学反应方程式的计算;有关溶质质量分数的简单计算.4016551 | |
| 专题: | 溶质质量分数与化学方程式相结合的计算. |
| 分析: | (1)二氧化锰作催化剂,反应前后质量不变; (2)反应前后锥形瓶中物质的质量差即为生成氧气的质量; (3)根据氧气的质量可以计算过氧化氢的质量,进一步可以计算过氧化氢溶液中溶质的质量分数. |
| 解答: | 解:(1)反应结束后,过滤,滤渣是二氧化锰,因为二氧化锰是催化剂,反应前后质量不变,所以滤渣的质量是1.0g. 故填:1.0. (2)生成氧气的质量为:20.0g+1.0g﹣20.2g=0.8g. 故填:0.8. (3)设过氧化氢的质量为X, 2H2O2 68 32 X 0.8g
X=1.7g, 过氧化氢溶液中溶质的质量分数为: 答:过氧化氢溶液中溶质的质量分数为8.5%. |
| 点评: | 差量法在计算中经常遇到,要掌握差量法计算的技巧,并且能够熟练运用,对解答计算方面的题目帮助很大. |

练习册系列答案
相关题目
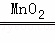 2H2O+O2↑,
2H2O+O2↑,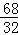 =
=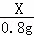 ,
,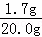 ×100%=8.5%;
×100%=8.5%;