题目内容
一定质量的某化合物完全燃烧,消耗9.6克氧气,生成8.8克二氧氧化碳和5.4克水.对该化合物的组成判断正确的是( )
A.只含有C、H两种元素
B.含有C、H、O三种元素
C.一定含有C、H两种元素,可能含有O元素
D.以上答案都不正确
【考点】质量守恒定律及其应用.
【专题】化学用语和质量守恒定律.
【分析】在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.
【解答】解:生成的二氧化碳和水中含有碳氢氧三种元素,根据质量守恒定律,碳元素和氢元素一定来自于化合物;
8.8克二氧化碳中,氧元素的质量为:8.8克×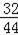
 =6.4g;
=6.4g;
5.4克水中,氧元素的质量为:5.4克×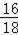
 =4.8g;
=4.8g;
二氧化碳和水中,氧元素的质量和为:6.4g+4.8g=11.2g>9.6g;
因此该化合物中还含有氧元素.
故选B.
【点评】在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案化学是一门以实验为基础的学科,请根据如图回答问题
|
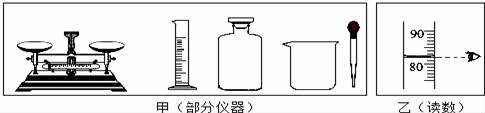
图甲 |
图乙 |
图丙 |
|
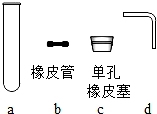
(1)图甲中:仪器a的名称是 .
(2)如果采用图乙的操作,可能造成的后果之一是 .
(3)利用图丙装置(夹持装置未画出)能进行的实验是 (填序号).
A、用高锰酸钾制氧气 B、用过氧化氢溶液与二氧化锰溶液制氧气
C、用锌和稀硫酸制氢气 D、用石灰石和稀盐酸制二氧化碳
请你写出用高锰酸钾制氧气的化学方程式: .
(4)图丙中的气体发生装置虽然简单、操作方便,但无法控制反应的进行.请从图丁中选取 (填序号)与图甲中a组成新的气体发生装置,已达到用时则开、不用时则关,控制反应进行的目的.
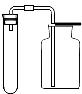
(5)如图所示的装置是一种可用于集气、洗气等的多功能装置,请回答下列问题:
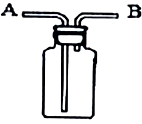
①若用排空气法收集CO2.则CO2气体应从装置的 端通入.
②若用排水法牧集h2,且h2从a端通入,可将该装置 .
③若用排水法收集O2,先将瓶内装滿水•,然后O2从 端通入;若需知道收集到O2的体积,可在另﹣端放一个 (填仪器名称)
(6)甲校的同学们在做CO还原CuO的实验时,各小组分别设计了以下四套实验装置.
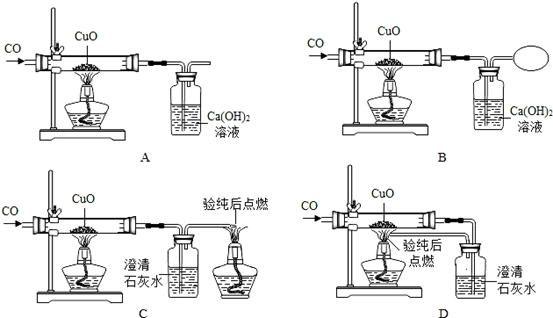
写出该实验澄清石灰水中发生的化学反应方程式: ,请你从防止空气污染、节约能源和安全操作的角度分析:最不理想的实验装置是 ,最合理的实验装置是 .
化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,具体方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,将体积换算为质量,再根据CO2的质量求出样品中碳酸钙的质量.如图Ⅰ为石灰石与稀盐酸反应的装置,图Ⅱ是用于测量CO2体积的装置.


(1)写出图中A、B仪器的名称:① ② ,检查A装置气密性的方法是 ,若在实验室中利用B装置制取氧气,化学反应方程式为 ,将B中装置②加装网罩,可以用于木炭还原氧化铜实验,反应的化学方程式为 ,该反应属于 (填基本反应类型);
(2)图Ⅰ装置为石灰石与稀盐酸反应的装置,应选择 (填“A”或“B”)图Ⅱ装置中油层的作用是 防 ,为使反应前后油层上方气体压强和外界大气压相同,可以采取的操作方法是 ,此时读数的变化即为生成二氧化碳的体积.
(3)下表是三个实验小组按方案所测得的数据.
| 小组 | 取用石灰石样品质量 | 测得CO2的质量 | 碳酸钙的质量分数 |
| 一 | 2.5g | 1.32g | 120% |
| 二 | 2.5g | 0.88g | ? |
| 三 | 2.5g | 1.1g | 100% |
Ⅰ第一、三小组测定结果明显偏高,可能的原因是 (填序号)
①盐酸浓度过高挥发出氯化氢;
②盐酸量不足;
③没有将发生装置内的二氧化碳完全排出
Ⅱ第二小组测定结果比较准确,根据数据计算石灰石中碳酸钙的质量分数.(写出计算过程)


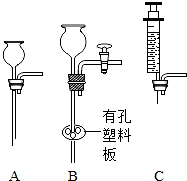 图丁
图丁 下列实验操作正确的是 ( )
下列实验操作正确的是 ( )