题目内容
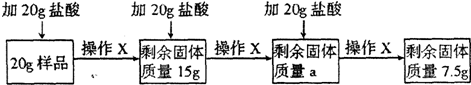
某兴趣小组的同学为分析一种石灰石样品中碳酸钙的质量分数,取20g样品放入烧杯,把60g稀盐酸分三次加入烧杯,使其充分反应(样品中所含杂质既不溶于水也不与稀盐酸反应),实验流程及数据如下(所有实验数据都不包括烧杯的质量,且不考虑
H2O和HCl的挥发;操作X包括搅拌、过滤、洗涤、干燥、称量):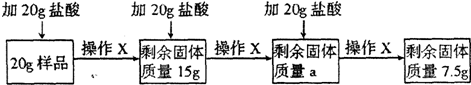
请回答:
(1)CaCO3中Ca与C的质量比为______;
(2)实验时判断已充分反应的现象是______:其中a为______g;样品中碳酸钙的质量分数为______;
(3)第三次反应过滤后所得溶液的pH______7(填“>”、“<”或“=”);为使该溶液显中性且得到尽可能多的CaCl2,最后可向烧杯中加入过量的______(填序号)
A.CaO B.CaCO3 C.Ca(OH)2 D.CaCl2
(4)计算所用稀盐酸中溶质的质量分数(写出计算过程)
解:(1)依据碳酸钙的化学式为CaCO3则可知Ca与C的质量比为40:12=10:3;
(2)碳酸钙与盐酸反应能生成二氧化碳,所以反应的现象为有气泡冒出,因此实验时判断已充分反应的现象是不再产生气泡,从第一次加入20g盐酸后固体变为15g,可知每20g盐酸能消耗5g碳酸钙,所以a值应该为15g-5g=10g,第三次加入20g盐酸后剩余固体是7.5g,不是10g-5g=5g,所以剩余的固体即为杂质,所以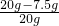 ×100%=62.5%;
×100%=62.5%;
(3)由(2)的分析可知完全反应后最终盐酸有剩余,所以溶液呈酸性,pH小于7,碳酸钙能与盐酸反应生成氯化钙、水、二氧化碳,二氧化碳作为气体会散失到空气中,氯化钙是需保留的物质,碳酸钙不溶于水,过量时可通过过滤除去,所以CaCO3最为合适,其它选项中A、C虽都能与盐酸反应但使用的量不好控制,量多则会导致溶液呈碱性,而D氯化钙不能与盐酸反应.
(4)设与10克碳酸钙反应的HCl的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
5g x
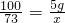
X=3.65g
所以稀盐酸中溶质的质量分数为: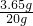 ×100%=18.25%.
×100%=18.25%.
故答案为:(1)10:3;(2)不再产生气泡;10;62.5%;(3)<;B;(4)18.25%;
分析:(1)依据化学式中元素的质量比等于原子的相对原子质量和的比分析解答;
(2)依据碳酸钙与盐酸反应会生成二氧化碳的现象判断充分反应的问题,根据各步反应消耗碳酸钙的质量分析a的数值,依据最终剩余的固体质量计算碳酸钙的质量分数;
(3)依据第三次加入盐酸后盐酸存在剩余的知识分析溶液的pH,依据消耗盐酸且生成较多氯化钙的知识分析加入的物质情况;
(4)依据数据分析可知20g盐酸能与5g碳酸钙恰好反应以及化学方程式的计算分析解答;
点评:分析实验所记录的数据时,注意数据变化量间的规律,利用变化规律判断完全反应时所涉及物质的质量.
(2)碳酸钙与盐酸反应能生成二氧化碳,所以反应的现象为有气泡冒出,因此实验时判断已充分反应的现象是不再产生气泡,从第一次加入20g盐酸后固体变为15g,可知每20g盐酸能消耗5g碳酸钙,所以a值应该为15g-5g=10g,第三次加入20g盐酸后剩余固体是7.5g,不是10g-5g=5g,所以剩余的固体即为杂质,所以
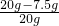 ×100%=62.5%;
×100%=62.5%;(3)由(2)的分析可知完全反应后最终盐酸有剩余,所以溶液呈酸性,pH小于7,碳酸钙能与盐酸反应生成氯化钙、水、二氧化碳,二氧化碳作为气体会散失到空气中,氯化钙是需保留的物质,碳酸钙不溶于水,过量时可通过过滤除去,所以CaCO3最为合适,其它选项中A、C虽都能与盐酸反应但使用的量不好控制,量多则会导致溶液呈碱性,而D氯化钙不能与盐酸反应.
(4)设与10克碳酸钙反应的HCl的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
5g x
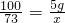
X=3.65g
所以稀盐酸中溶质的质量分数为:
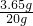 ×100%=18.25%.
×100%=18.25%.故答案为:(1)10:3;(2)不再产生气泡;10;62.5%;(3)<;B;(4)18.25%;
分析:(1)依据化学式中元素的质量比等于原子的相对原子质量和的比分析解答;
(2)依据碳酸钙与盐酸反应会生成二氧化碳的现象判断充分反应的问题,根据各步反应消耗碳酸钙的质量分析a的数值,依据最终剩余的固体质量计算碳酸钙的质量分数;
(3)依据第三次加入盐酸后盐酸存在剩余的知识分析溶液的pH,依据消耗盐酸且生成较多氯化钙的知识分析加入的物质情况;
(4)依据数据分析可知20g盐酸能与5g碳酸钙恰好反应以及化学方程式的计算分析解答;
点评:分析实验所记录的数据时,注意数据变化量间的规律,利用变化规律判断完全反应时所涉及物质的质量.

练习册系列答案
相关题目
某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
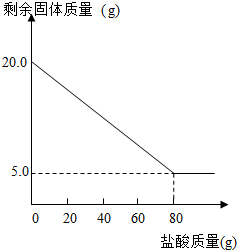
请细心观查表格和图象,回答下列问题:
(1)涉及反应的化学方程式为 ;
(2)第 次石灰石中的碳酸钙与盐酸恰好反应完毕;
(3)该石灰石样品中碳酸钙的质量分数为 ;
(4)表格中m= g;
(5)该样品完全反应生成二氧化碳的质量是 g.
| 实验次数 | 稀盐酸的用量(g) | 剩余固体的质量(g) |
| ① | 20 | 16.25 |
| ② | 40 | 12.50 |
| ③ | 60 | M |
| ④ | 80 | 5.00 |
| ⑤ | 100 | 5.00 |

请细心观查表格和图象,回答下列问题:
(1)涉及反应的化学方程式为
(2)第
(3)该石灰石样品中碳酸钙的质量分数为
(4)表格中m=
(5)该样品完全反应生成二氧化碳的质量是
(8分)某兴趣小组的同学为分析一种石灰石样品中碳酸钙的质量分数,取20g样品放入烧杯,把60g稀盐酸分三次加入烧杯,使其充分反应(样品中所含杂质既不溶于水也不与稀盐酸反应),实验流程及数据如下(所有实验数据都不包括烧杯的质量,且不考虑H2O和HCl的挥发;操作X包括搅拌、过滤、洗涤、干燥、称量):

请回答:
(1)CaCO3中Ca与C的质量比为 ;
(2)实验时判断已充分反应的现象是 :其中a为 g;样品中碳酸钙的质量分数为 ;
(3)第三次反应过滤后所得溶液的pH 7(填“>”、“<”或“=”);为使该溶液
显中性且得到尽可能多的CaCl2,最后可向烧杯中加入过量的 (填序号)
(4)计算所用稀盐酸中溶质的质量分数(写出计算过程)

请回答:
(1)CaCO3中Ca与C的质量比为 ;
(2)实验时判断已充分反应的现象是 :其中a为 g;样品中碳酸钙的质量分数为 ;
(3)第三次反应过滤后所得溶液的pH 7(填“>”、“<”或“=”);为使该溶液
显中性且得到尽可能多的CaCl2,最后可向烧杯中加入过量的 (填序号)
| A.CaO | B.CaCO3 | C.Ca(OH)2 | D.CaCl2 |
 某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下:
某兴趣小组的同学为测定某石灰石中碳酸钙(假设:石灰石中的杂质不与盐酸反应)的质量分数,称取一定质量的石灰石置于烧杯中,用某浓度的稀盐酸100g,分5次加入,每次充分反应后,取出固体,经过滤、洗涤、干燥等操作后称重,各次稀盐酸用量和剩余固体质量记录如下: