题目内容
19.用化学方程式表示除去下列物质中少量杂质的过程(括号内为杂质):(1)H2(CO2)CO2+2NaOH═Na2CO3+H2O
(2)CaCl2(CaCO3)CaCO3+2HCl═CaCl2+H2O+CO2↑
(3)FeCl2(CuCl2)Fe+CuCl2=FeCl2+Cu
(4)CaO(CaCO3)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)CO2能与氢氧化钠溶液反应生成碳酸钠和水,氢气不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
(2)碳酸钙能与适量的稀盐酸反应生成氯化钙、水和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)要除去FeCl2溶液中的CuCl2,实质就是除去铜离子,可利用CuCl2溶液与足量的铁粉反应生成氯化亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuCl2=FeCl2+Cu.
(4)碳酸钙高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
故答案为:(1)CO2+2NaOH═Na2CO3+H2O;(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;(3)Fe+CuCl2=FeCl2+Cu;(4)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
10. 小军以木条为基本原料,进行了如下一系列探究实验:
小军以木条为基本原料,进行了如下一系列探究实验:
(1)对木条组成的探究:
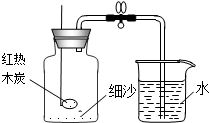
(2)小军根据燃烧红磷测定空气中氧气含量的实验原理,认为可用木条燃烧产生的木炭代替红磷测定空气中氧气的含量,并按如图装置进行实验.
①依据的实验原理是木炭燃烧消耗氧气
小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象.
经过认真分析,小军发现实验失败的原因是(答一条)木炭燃烧虽消耗了氧气,但产生了新的气体,致使集气瓶内气体压强未减少
②小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条)药品要在空气中燃烧.
 小军以木条为基本原料,进行了如下一系列探究实验:
小军以木条为基本原料,进行了如下一系列探究实验:(1)对木条组成的探究:
| 实验操作 | 实验现象 | 实验结论 | 方法提炼 |
| 点燃干燥的木条,在火焰上方罩一干燥的冷烧杯 | 一会儿烧杯内壁有水雾产生. | 木条中一定含有氢元素 | 根据实验现象 可以推测出实验结论. |
| 继续把火焰靠近烧杯底部 | 一会儿烧杯底部出现一层黑色物质 | 木条中一定含有碳元素 |
①依据的实验原理是木炭燃烧消耗氧气
小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入集气瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,打开弹簧夹,并未发现倒吸现象.
经过认真分析,小军发现实验失败的原因是(答一条)木炭燃烧虽消耗了氧气,但产生了新的气体,致使集气瓶内气体压强未减少
②小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是(答一条)药品要在空气中燃烧.
8.向硝酸银、硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤液中滴加稀盐酸有白色沉淀产生,下列说法正确的是( )
| A. | 所得滤液中可能含有Cu2+ | |
| B. | 所得滤渣中可能含有Cu | |
| C. | 所得滤液中一定含有Ag+、Cu2+、Fe2+ | |
| D. | 所得滤渣中一定含有Ag和Cu |

 的粒子Cl-
的粒子Cl-