题目内容
5.请根据如图所示的实验室中实验装置图填空.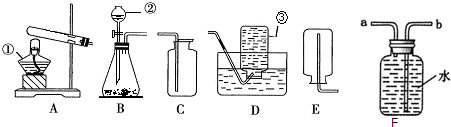
(1)完成图中标有数字的仪器的名称:①酒精灯②分液漏斗 ③集气瓶.
(2)组装好B装置后,先向分液漏斗中加入水,然后将导管一端通入水中,并打开分液漏斗的活塞,观察导管口是否有连续的气泡冒出,该操作的目的是检查装置气密性.
(3)用高锰酸钾制备氧气的发生装置应选A,写出反应化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.①可用图D所示的方法收集氧气,主要是因为氧气不易溶于水.
②应将收集满氧气的氧气瓶正放在桌面上.
③用图9所示装置收集氧气,氧气应从a(填“a”或“b”)端导入.
(4)在实验室中,制取并收集二氧化碳选用装置为B和C(填字母编号),反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(5)要鉴别氧气和二氧化碳,可选择ABC.
A.紫色石蕊溶液 B.澄清石灰水 C.燃着的木条.
分析 (1)从仪器的图和用途去分析解答;
(2)从组装好A装置后,要先检查装置的气密性,防止由于漏气而收集不到制取的气体,造成药品的浪费去分析解答;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;氧气的密度比空气的密度大,不易溶于水;
(4)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳; 二氧化碳能够溶于水,密度比空气大,不能燃烧,不支持燃烧.
(5)根据氧气与二氧化碳的化学性质的不同点进行区分.
解答 解:(1)由仪器的图和用途可知①酒精灯; ②分液漏斗;③集气瓶;
(2)组装好B装置后,要先检查装置的气密性,防止由于漏气而收集不到制取的气体,造成药品的浪费,所以该同学先向分液漏斗中加入水,然后将导管一端通入水中,并打开分液漏斗的活塞,观察导管口是否有连续的气泡冒出,该操作的目的是检查装置的气密性;故答案为:检查装置的气密性;
(3)实验室用高锰酸钾制取氧气时需要加热,应选择的气体发生装置是A装置,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
①可用D装置收集氧气是因为氧气不易溶于水;
②由于氧气的密度比空气大,所以收集满氧气的氧气瓶应正放在桌面上;
③由于氧气的密度比水的密度小,从短管a进;
(4)实验室制取二氧化碳时不需要加热,应选择的气体发生装置是B装置,反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用C装置收集;
(5)二氧化碳能使燃着的木条熄来,通入紫色石蕊试液中紫色石蕊试液变红,能使澄清石灰水变浑浊,而氧气与二氧化碳都不能使酚酞变色,故选ABC.
答案:(1)①酒精灯; ②分液漏斗;③集气瓶.
(2)检查装置气密性.
(3)A,2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.①不易溶于水.②正.③a.
(4)B,C,CaCO3+2HCl=CaCl2+H2O+CO2↑.
(5)ABC.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,是中考的重要考点之一,主要出现在实验题中.

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案| A. |  钛合金制人造骨 | B. |  形状记忆合金做人造卫星天线 | ||
| C. |  宝石中含有某些金属使其绚丽多彩 | D. |  用锰钢做自行车架 |
| 物 质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 7 | 0 | 3 |
| A. | 升高温度,三溶液中溶质的质量分数一定会改变 | |
| B. | 三溶液中溶质的质量分数乙>丙>甲 | |
| C. | 所得溶液可能都是饱和溶液 | |
| D. | 20℃时,甲的溶解能力最小 |
某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
【查阅资料】
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液呈碱性 | 水溶液呈碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
实验一:探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变红色,但食用纯碱溶液中颜色更深,由此推测可能食用纯碱溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用pH试纸进行测定.
实验二:比较两种物质的热稳定性
设计如图(1)装置:小试管套装在带有支管的大试管中,整套装置气密性好,其他装置略去.
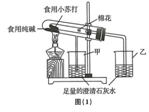 (1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.
(1)为确保安全,实验结束时,在撤离酒精灯前必须完成的操作是把A、B试管中的导管移出液面.(2)现象与结论:装有碳酸氢钠的试管口生成较多的无色小液滴,同时烧杯乙中有大量的气泡产生,澄清石灰水变浑浊;烧杯甲中也有气泡产生,澄清石灰水没有明显变化;实验结束后,经检验大、小两试管内的物质均是碳酸钠.结合以上实验,可得出结论:①碳酸氢钠受热生成的物质是碳酸钠、水和二氧化碳.②在受热条件下,碳酸钠比碳酸氢钠稳定.
实验三:比较与盐酸反应生成相同体积二氧化碳气体的快慢
取碳酸氢钠4.2g放入如图Ⅰ装置的锥形瓶中,取碳酸钠5.3g放入另一相同装置的锥形瓶中,分别加入相同质量、相同浓度的盐酸(足量).相同的条件下,通过图Ⅱ装置测量出生成气体的体积,得到时间-体积关系曲线如图Ⅲ所示.
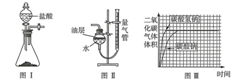
(4)已知二氧化碳不溶于该油层,图Ⅱ装置中油层的作用是防止部分的二氧化碳溶于水,造成实验误差.
(5)数据与分析:根据图Ⅲ曲线,可得出有关“比较与盐酸反应生成相同体积二氧化碳气体的快慢”的结论是在相同的条件下生成相同体积的二氧化碳,碳酸氢钠与盐酸反应比碳酸钠与盐酸反应快.
(6)反思与讨论:实验中“取碳酸氢钠4.2g、碳酸钠5.3g”的目的是生成相同体积的二氧化碳.
(1)提出问题:你提出的问题是:用酒精灯给物质加热时,应该用哪一层火焰?
(2)作出猜想:你的猜想是用酒精灯外焰给物质加热
(3)实验过程和记录:取出三支试管,各加入3mL的水.1、其中一支试管的底部放在火焰上方3cm处.2、将另一支试管的底部与灯芯接触加热.3、第三支试管的底部放在外焰部分加热.记录上述情况下将水加热至沸腾时所需时间如下:
| 情况1 | 情况2 | 情况3 | |
| 所需时间 | 87s | 54s | 25s |
| 结论 | |||
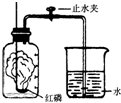 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: