题目内容
9. 工业上以大理石和赤铁矿主要成分为A和F为主要原料可以制取B和G,其转化关系如图所示,
工业上以大理石和赤铁矿主要成分为A和F为主要原料可以制取B和G,其转化关系如图所示,已知D为非金属单质,G为金属单质,H为最常见的氧化物.
试回答下列问题:
(1)写出工业制取的两种物质的化学式:BCaCl2、GFe.
(2)写出下列反应的化学方程式:
反应②:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
反应③:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
检验气体C:CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据题干提供的信息进行分析,结合图框,根据“工业上以大理石和赤铁矿主要成分为A和F为主要原料可以制取B和G”,物质A与稀盐酸反应生成B、C、H,C与D高温生成E,而E与F反应生成G和C,所以A为碳酸钙、F为氧化铁,结合“D为非金属单质,G为金属单质,H为最常见的氧化物”,又因为C可以与单质D在高温下反应,因此可判断C为二氧化碳、B为氯化钙、H为水,D为碳单质;则E、F为一氧化碳还原氧化铁生成物质C二氧化碳和单质G为铁,代入检验.
解答 解:根据“工业上以大理石和赤铁矿主要成分为A和F为主要原料可以制取B和G”,结合图框,物质A与稀盐酸反应生成B、C、H,C与D高温生成E,而E与F反应生成G和C,所以A为碳酸钙、F为氧化铁,结合“D为非金属单质,G为金属单质,H为最常见的氧化物”,又因为C可以与单质D在高温下反应,因此可判断C为二氧化碳、B为氯化钙、H为水,D为碳单质;则E、F为一氧化碳还原氧化铁生成物质C二氧化碳和单质G为铁,代入检验,符合题意.
(1)物质B为氯化钙,G为铁,所以工业制取的两物质分别为氯化钙和铁;故CaCl2,Fe;
(2)反应②为单质碳在高温下与二氧化碳反应生成一氧化碳;故其化学方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
反应③为工业炼铁的原理反应,一氧化碳还原氧化铁,生成铁和二氧化碳;故其化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
气体C为二氧化碳,因此可通入澄清石灰水进行检验,石灰水变浑浊;故其化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:
(1)CaCl2,Fe;
(2)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

| A.物质的分类 | B.资源的利用和保护 |
| ①氧化物-一定含有氧元素 ②混合物-一定含有多种元素 | ①保护空气一减少有害气体和烟尘的排放 ②爱护水资源一节约用水和防止水体污染 |
| C.性质与用途 | D.用“化学”眼光分析 |
| ①石墨能导电--作铅笔芯 ②活性炭有吸附性--作冰箱除臭剂 | ①湿衣服晾干一分子之间有间隔 ②明矾净水一明矾溶于水生成胶状物 |
| A. | A | B. | B | C. | C | D. | D |
| A. |  | B. | 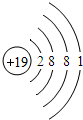 | C. |  | D. | 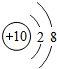 |
| A. | 60g | B. | 5 0g | C. | 40g | D. | 30g |
| A. | 4Fe+3O2═2Fe2O3 | B. | H2O2═H2↑+O2 | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | C+O2═CO2 |
| A. | 将河水经过沉淀、过滤、活性炭吸附等净化处理后,所得的水就是纯水 | |
| B. | 水是一种常见的溶液 | |
| C. | 煮沸可以降低自来水的硬度 | |
| D. | 电解水实验说明水是由氢气和氧气组成的 |
| A. | 23 | B. | 27 | C. | 40 | D. | 56 |
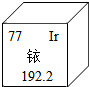 南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )
南京某公司丢失一枚探伤用放射源铱-192,经多方寻找终于放回安 全箱.右图是元素周期表提供的铱元素的部分信息,下列说法正确的是( )| A. | 铱的原子序数为115 | B. | 铱原子的核电荷数为77 | ||
| C. | 铱的相对原子质量为192.2g | D. | 铱原子的核内中子数为80 |
 “践行绿色生活”被确定为2015年世界环境日的中国主题.下列做法符合这一主题的是( )
“践行绿色生活”被确定为2015年世界环境日的中国主题.下列做法符合这一主题的是( )| A. | 直接焚烧秸秆 | B. | 大量使用农药化肥 | ||
| C. | 不断提高汽车尾气净化技术 | D. | 工厂废水任意排放 |