题目内容
16.现有100g 10%的食盐溶液,要使其质量分数变为20%,有三种方法,请按不同的转变方法进行计算:(1)继续加入食盐,其质量为多少g?
(2)蒸发水分,其质量为多少g?
(3)若混入25%的食盐溶液,其溶液质量为多少g?
分析 (1)根据稀溶液中溶质的质量与继续加入食盐的质量的和等于浓溶液中溶质的质量来列式解答;
(2)根据溶液在蒸发前后溶质的质量不变来列等式解答;
(3)根据两份溶液在混合时溶质的质量之和等于所得溶液中溶质的质量来解答.
解答 解:(1)设继续加入的食盐的质量为x,
则100g×10%+x=(100g+x)×20%
解得x=12.5g
(2)设蒸发水的质量为y,
则根据蒸发前后溶质的质量不变得,
100g×10%=(100g-y)×20%
解得y=50g
(3)设质量分数为25%的溶液为z,
则10%的溶液中的溶质与25%的溶液中的溶质之和等于20%溶液中的溶质,
100g×10%+z×25%=(100g+z)×20%
解得z=200g
故答案为:(1)12.5;(2)50;(3)200.
点评 本题考查了三种增大溶液质量分数的方法及其计算,学生需要明确不同方法中变化的量和不变的量,明确溶质的关系来解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列说法正确的是( )
| A. | 分子的质量大,原子的质量小 | |
| B. | 分子之间有间隔,原子之间没有间隔 | |
| C. | 在化学反应中,分子可分,原子不可分 | |
| D. | 分子可直接构成物质,原子不能直接构成物质 |
8.向硝酸银、硝酸铜的混合溶液中加入一些铁粉,等完全反应后再过滤.下列情况不可能出现的是( )
| A. | 滤纸上若有Ag,滤液中可能有有Fe2+、Cu2+、Ag+ | |
| B. | 滤纸上若有Ag、Cu,滤液中不可能有Ag+ | |
| C. | 滤纸上若有Ag、Cu、Fe,滤液中一定只有Fe2+ | |
| D. | 滤纸上若有Ag、Cu、Fe,滤液中可能有Cu2+、Ag+ |
 某补钙药剂的标签主要内容如图所示,为测定该钙片含量是否符合标注,做如下实验:取10片该钙片粉碎,放人干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的总质量为64.5g.
某补钙药剂的标签主要内容如图所示,为测定该钙片含量是否符合标注,做如下实验:取10片该钙片粉碎,放人干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的总质量为64.5g.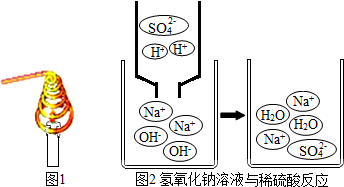
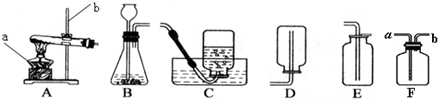
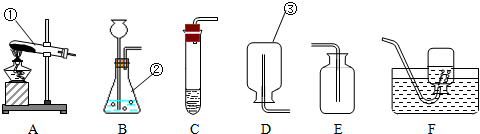
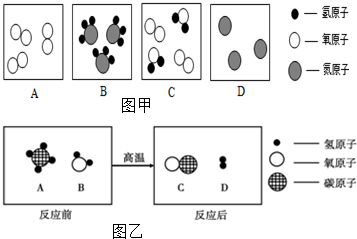 在宏观、微观和符号之间建立联系是化学学科的特点.
在宏观、微观和符号之间建立联系是化学学科的特点.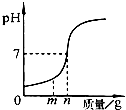 用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,往所得溶液中滴加紫色石蕊溶液,溶液呈红色.
用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰mg时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,往所得溶液中滴加紫色石蕊溶液,溶液呈红色.