题目内容
6.分别用一种试剂除去下列溶液中的少量杂质(括号内物质是杂质).用化学方程式回答:①HNO3(HCl)AgNO3+HCl═AgCl↓+HNO3;
②NaCl(Na2SO4)Na2SO4+BaCl2═BaSO4↓+2NaCl.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:①要除去HNO3中的HCl,实质就是除去氯离子,可利用HCl与硝酸银溶液反应生成氯化银沉淀和硝酸,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
②要除去NaCl溶液中的Na2SO4,实质就是除去硫酸根离子,可利用Na2SO4溶液与氯化钡溶液反应生成硫酸钡沉淀和氯化钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Na2SO4+BaCl2═BaSO4↓+2NaCl.
故答案为:①AgNO3+HCl═AgCl↓+HNO3;②Na2SO4+BaCl2═BaSO4↓+2NaCl.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
17.下列实验操作与预期实验目的或所得实验结论一致的是( )
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 向1,2两试管中分别加入等浓度H2O2溶液10mL、1mL,再向H2O2溶液中分别滴入等浓度等体积CuSO4、FeCl3溶液;试管2中产生气体较快 | 证明FeCl3溶液的催化效率 更高 |
| B | 将洁净的铁钉在饱和食盐水中浸泡一段时间;铁钉上有气泡产生 | 证明铁发生析氢腐蚀 |
| C | 测定物质的量浓度相同的盐酸和醋酸溶液的pH;盐酸pH小于醋酸pH | 证明盐酸酸性比醋酸强 |
| D | 硅酸钠溶液中滴入酚酞,溶液变红,再滴加稀盐酸,溶液红色变浅直至消失 | 证明非金属性:Cl>Si |
| A. | A | B. | B | C. | C | D. | D |
14.电离时,一定相等的是( )
| A. | 每个阴、阳离子所带电荷 | B. | 阴、阳离子个数 | ||
| C. | 阴、阳离子所带电荷总数 | D. | 以上说法中都不对 |
11.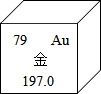 如图是金元素在元素周期表中的信息示意图.从图中获取的信息正确的是( )
如图是金元素在元素周期表中的信息示意图.从图中获取的信息正确的是( )
 如图是金元素在元素周期表中的信息示意图.从图中获取的信息正确的是( )
如图是金元素在元素周期表中的信息示意图.从图中获取的信息正确的是( )| A. | 金元素属于非金属元素 | B. | 一个金原子的中子数为197 | ||
| C. | 一个金原子质子数为79 | D. | 一个金原子的核外电子数为118 |
18.溶液在生产、生活中起着十分重要的作用.下列有关溶液的说法中,正确的是( )
| A. | 不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 | |
| B. | 饱和溶液析出晶体后,溶质的质量分数一定减小 | |
| C. | 只要温度不变,某饱和溶液中固体溶质的溶解度一定不变 | |
| D. | 降温时,饱和溶液一定会析出晶体 |
15.小玲同学对所学部分化学知识归纳如下,其中有错误的一组是( )
| A.生活中的物质 | B.安全常识 | C.元素与人体健康 | D.日常生活经验 |
| 铅笔芯主要成分--石墨 饮水机滤芯的吸附剂主要成分--活性炭 | 进入陌生溶洞前--先做灯火实验 闻试剂气味--鼻子尽量靠近试剂瓶口 | 缺铁--易引起贫血 缺碘--易患甲状腺肿大 | 区别老陈醋与酱油--闻气味 区分羊毛纤维与合成纤维-灼烧后闻气味 |
| A. | A | B. | B | C. | C | D. | D |
16.以保护环境和垃圾资源化为目的,将城市生活垃圾进行分类,下列垃圾属于同类物质的( )
| A. | 废电池、易拉罐 | B. | 废铜烂铁、塑料袋 | ||
| C. | 废旧报纸、硬纸板 | D. | 包装塑料、空啤酒瓶 |
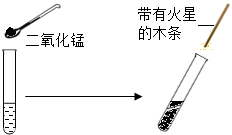 小华学习了双氧水(过氧化氢俗称双氧水)制氧气的实验后,想起自己家里也有一瓶消毒用双氧水,由于标签已部分受损无法判断是否变质,他将该瓶溶液带到学校,进行了如图所示的探究.试回答:
小华学习了双氧水(过氧化氢俗称双氧水)制氧气的实验后,想起自己家里也有一瓶消毒用双氧水,由于标签已部分受损无法判断是否变质,他将该瓶溶液带到学校,进行了如图所示的探究.试回答: