��Ŀ����
5�� ����ȫ����Сѧ����ȫ�����Ļ����Ϊ����ǿ���ּ��֣�������гУ��������ѧУ��Χ����һ���չ����ʽ�����ġ�֪ʶ�ػ���������ȫ�������
����ȫ����Сѧ����ȫ�����Ļ����Ϊ����ǿ���ּ��֣�������гУ��������ѧУ��Χ����һ���չ����ʽ�����ġ�֪ʶ�ػ���������ȫ�������������δȻ
��1�������ߵ�ϣ����ֹ����������ֵķ���ԭ���ֱ��DZ���ʹ��ȼ����¶ȴﵽ���Ż������ȼ�
��2��һ��Ȥζʵ������ߵ�������Ϩ���Ҳ豭�ڱڱ�ڣ�
��ʾ�����Ż�ķ�������ʱӦ�ø�������ʪë����ڱ����룮
��3������Ҳ�Ƿ��ֵ�һ����Ҫ���ݣ���Խ������ҹ�һЩ�������ֵ�����ڲ����飬���ǿ���������������Ϊ0.3%�Ĺ������ᣨ��ѧʽC2H4O3�����ճ��þ߽�������������0.3%�Ĺ���������Һ500g����Ҫ15%�Ĺ���������Һ10g��
�����ؽ�
��4������ʳƷ����Ҫ�ľ�������֮һ������Сѧ��ͬѧΪij�����������˷����桢���ȳ�����Ȫˮ�ȷ���ʳƷ���Ӿ���Ӫ���ĽǶȿ�����Ӧ���ӵ�ʳƷ���߲ˡ�ˮ����
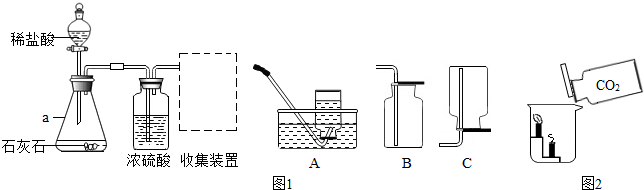
��5�����鷢�����������й��ࡢ��ȣ�Ҫ��ʱ����������ͨ��������ʯ�Ұ�1��1�ı���������ȴ�������ʱ���ܷ�����һ����ѧ��Ӧ����ʽΪCaO+H2O=Ca��OH��2��
��6����ʯ����ʹ�ù����У������ᷢ����������ȡ10g�Ѳ��ֱ��ʵ���ʯ����Ʒ���������ʽ�Ϊ̼��ƣ��һ�Ͼ��ȣ��������л�������100g30%�����ᣨ����������ַ�Ӧ����������ȫ�ų�������Ӧʣ��Һ�������Ϊ107.8g�������Ʒ����ʯ�ҵ�����������
���� ��1������ȼ�����������ԭ��������
��2������������Ϣ�к����弰�̳����Ϸ�������
��3������ϡ��ǰ�������������������
��4������������������Ӫ���ط�����
��5��������ʯ�ҵĻ�ѧ���ʷ�����
��6�����������غ㶨�ɷ�Ӧǰ�������ʵ������Ϊ���ɵĶ�����̼�����������ݻ�ѧ����ʽ���̼��Ƶ����������������Ʒ����ʯ�ҵ�����������
��� �⣺��1������ȼ�յ������ǿ�ȼ��������Ӵ����¶ȴﵽ�Ż�㣬����ȱһ���ɣ��ƻ�ȼ������֮һ���ɴﵽ��𣮡����ߵ�ϡ��DZ���ʹ��ȼ���¶ȴﵽ�Ż���ȼ�գ������ֹ������Ǹ����ȼ�
��2���Ż�ķ������ȵ��к����弰�̳��ڸߴ������Ż�ķ�������ʱӦ�ø������Ӳ���ʪë����ס�ڱ����룮
��3������ϡ��ǰ�������������䣬����15%�Ĺ���������Һ������Ϊx����0.3%��500g=15%��x
x=10g
��4��������������Ӫ�������ࡢ�����ʡ���֬��ά���ء�ˮ�����Σ��������к������࣬���ȳ��к��е����ʺ���֬����Ȫˮ�к���ˮ�����Σ��Ӿ���Ӫ���ĽǶȿ�����ȱ��ά���أ�Ӧ���ӵĺ���ά���ص�ʳƷ�����߲ˡ�ˮ����
��5�����鷢�����������й��ࡢ��ȣ�Ҫ��ʱ����������ͨ��������ʯ�Ұ�1��1�ı���������ȴ�������ʱ��ʯ����ˮ�������Ϸ�Ӧ�����������ƣ��������ƿ�ɱ����������ѧ��Ӧ����ʽΪCaO+H2O=Ca��OH��2
��6�����������غ㶨�ɣ���Ӧ���ɵĶ�����̼������Ϊ10g+100g-107.8g=2.2g
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
x 2.2g
$\frac{100}{x}=\frac{44}{2.2g}$
x=5g
��Ʒ����ʯ�ҵ���������=$\frac{10g-5g}{10g}$��100%=50%
����Ʒ����ʯ�ҵ���������Ϊ50%
�ʴ�Ϊ����1������ʹ��ȼ����¶ȴﵽ���Ż������ȼ�
��2����������ʪë����ڱ����룮
��3��10g��
��4���߲ˡ�ˮ����
��5��CaO+H2O=Ca��OH��2��
��6��50%
���� ���⿼����������صĻ�ѧ֪ʶ��������ȼ�������ԭ������Һ��ϡ�ͣ�����Ӫ�����Լ���ѧ����ʽ�ļ��㣬�����֪ʶ��϶࣬���е��⣮

| A�� | �з��ⷢ�ȵ�һ����ȼ�� | |
| B�� | ȼ��һ���л��� | |
| C�� | ȼ��һ���л�ѧ�仯 | |
| D�� | Ҫʹ��Ϩ�𣬱���ʹ��ȼ���������������ʹ�¶Ƚ����Ż������ |
| A�� | 48��32��80 | B�� | 24��32��40 | C�� | 24��32��64 | D�� | 24��32��80 |
| A�� | пƬ��ϡ�������ܽ� | B�� | �������ú������� | ||
| C�� | Ũ����ʹСľ����� | D�� | ����ʯ��ˮ����� |
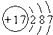 ��ʾAl��
��ʾAl��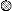 ����ʾһ����ԭ�ӣ���
����ʾһ����ԭ�ӣ���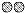 ����ʾ2N��
����ʾ2N��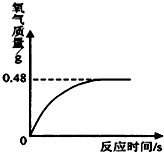 ����������Һ���ڱ������Ȼ�ֽ⣮С���Ӽ�������һƿ���õ�ҽ�ù���������Һ����ͬѧ��һ����ȡ����������ȡ������Һ51g�����������������̣����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ��
����������Һ���ڱ������Ȼ�ֽ⣮С���Ӽ�������һƿ���õ�ҽ�ù���������Һ����ͬѧ��һ����ȡ����������ȡ������Һ51g�����������������̣����������������뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ��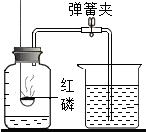 ij��ͬѧ����ͼװ�òⶨ�����������ĺ��������õ��ɼм�ס�齺�ܣ���ȼ���ף�����ƿ�в�����ƿ����������Ϩ����ȴ���ɼУ��۲���ƿ��ˮ��仯�����ʵ����ϣ���ͬѧ�Ĺ��ƿ��ˮ���������Դ���ƿ�ڿ��������$\frac{1}{5}$����ͬѧ�Ĺ��ƿ��ˮ����������С��ƿ�ڿ��������$\frac{1}{5}$�����ж�������������ͺ������ǣ�������
ij��ͬѧ����ͼװ�òⶨ�����������ĺ��������õ��ɼм�ס�齺�ܣ���ȼ���ף�����ƿ�в�����ƿ����������Ϩ����ȴ���ɼУ��۲���ƿ��ˮ��仯�����ʵ����ϣ���ͬѧ�Ĺ��ƿ��ˮ���������Դ���ƿ�ڿ��������$\frac{1}{5}$����ͬѧ�Ĺ��ƿ��ˮ����������С��ƿ�ڿ��������$\frac{1}{5}$�����ж�������������ͺ������ǣ�������