题目内容
甘油在印刷、化装品等工业中常用作润湿剂,也可以用来制造医药和炸药.
(1)根据甘油的化学式C3H8O3,你能得出哪些信息?(任写两个)
① ;
② ;
(2)在计算C3H8O3的相对分子质量,我会选择下面计算格式中的
A.C3H8O3=12×3+8+16×3=94
B.C3H8O3=C×3+H×8+O×3=12×3+8+16×3=94
C.C3H8O3的相对分子质量=12×3+8+16×3=94
D.C3H8O3的相对分子质量=3C+8H+3O=94
(3)在计算C3H8O3中氢元素的质量分数,我会选择下面计算格式中的
A.
×100%
B.
×100%
C.
D.
×100%
(4)瑞典化学家诺贝尔是安全使用硝化甘油炸药的第一人.硝化甘油(C3H5N3O9)是意大利化学家索布赖罗利用甘油和某物质X在一定的条件下合成的,该反应的化学方程式是C3H8O3+3X=C3H5N3O9+3H2O.则X的化学式是 .
(1)根据甘油的化学式C3H8O3,你能得出哪些信息?(任写两个)
①
②
(2)在计算C3H8O3的相对分子质量,我会选择下面计算格式中的
A.C3H8O3=12×3+8+16×3=94
B.C3H8O3=C×3+H×8+O×3=12×3+8+16×3=94
C.C3H8O3的相对分子质量=12×3+8+16×3=94
D.C3H8O3的相对分子质量=3C+8H+3O=94
(3)在计算C3H8O3中氢元素的质量分数,我会选择下面计算格式中的
A.
| 8H |
| C3H8O3 |
B.
| H的相对原子质量 |
| C3H8O3相对分子质量 |
C.
| H的相对原子质量×8 |
| C3H8O3相对分子质量 |
D.
| H的相对原子质量×8 |
| C3H8O3相对分子质量 |
(4)瑞典化学家诺贝尔是安全使用硝化甘油炸药的第一人.硝化甘油(C3H5N3O9)是意大利化学家索布赖罗利用甘油和某物质X在一定的条件下合成的,该反应的化学方程式是C3H8O3+3X=C3H5N3O9+3H2O.则X的化学式是
考点:化学式的书写及意义,相对分子质量的概念及其计算,元素的质量分数计算,质量守恒定律及其应用
专题:化学式的计算,化学用语和质量守恒定律
分析:(1)根据化学式的意义来分析;(2)根据相对分子质量的计算方法来分析;(3)根据化合物中某元素的质量分数计算方法来分析;(4)根据质量守恒定律来分析解答.
解答:解:(1)根据甘油的化学式C3H8O3可知,甘油由C、H、O三种元素组成,每个甘油分子中有3个C原子,8个H原子,3个O原子,甘油分子中C、H、O原子个数比为3:8:3,甘油中C、H、O元素质量比为9:2:12.
(2)根据相对分子的质量为组成分子的各原子的质量之和,甘油的相对分子质量为12×3+1×8+16×3=92.
(3)物质中某元素的质量分数=
×100%,甘油 C3H8O3中氢元素的质量分数=
×100%;
(4)根据C3H8O3+3X═C3H5N3O9+3H2O可知,
反应前:有3个碳原子、6个氢原子、3个氧原子,反应后:有3个碳原子、11个氢原子、12个氧原子和3个氮原子,且X前面的化学计量数为3,则每个X中含有1个氢原子、1个氮原子、3个氧原子,是硝酸.
故答案为:(1)①甘油由三种元素组成;②一个甘油分子含有14个原子;③在甘油中碳、氢、氧三种元素的质量比为9:8:12;④甘油是一种有机化合物;
(2)C;
(3)D;
(4)HNO3
(2)根据相对分子的质量为组成分子的各原子的质量之和,甘油的相对分子质量为12×3+1×8+16×3=92.
(3)物质中某元素的质量分数=
| 该元素相对原子量×原子个数 |
| 该物质的相对分子质量 |
| 氢的相对原子质量×氢原子个数 |
| 甘油的相对分子质量 |
(4)根据C3H8O3+3X═C3H5N3O9+3H2O可知,
反应前:有3个碳原子、6个氢原子、3个氧原子,反应后:有3个碳原子、11个氢原子、12个氧原子和3个氮原子,且X前面的化学计量数为3,则每个X中含有1个氢原子、1个氮原子、3个氧原子,是硝酸.
故答案为:(1)①甘油由三种元素组成;②一个甘油分子含有14个原子;③在甘油中碳、氢、氧三种元素的质量比为9:8:12;④甘油是一种有机化合物;
(2)C;
(3)D;
(4)HNO3
点评:本题难度不大,考查同学们灵活运用化学式的有关计算以及质量守恒定律进行分析问题、解决问题的能力.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
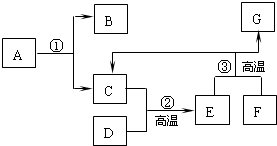 A~F都是初中化学中常见的物质,已知A是可乐等饮料中常见的一种物质.D和F都是黑色固体,D、G的主要成分为单质.C、E为气体,且C是光合作用的原料.试回答下列问题:
A~F都是初中化学中常见的物质,已知A是可乐等饮料中常见的一种物质.D和F都是黑色固体,D、G的主要成分为单质.C、E为气体,且C是光合作用的原料.试回答下列问题: