题目内容
若鸡蛋中碳酸钙的质量分数为50%,高温煅烧100kg鸡蛋壳使其完全分解(其中杂质不产生二氧化碳),
(1)可产生二氧化碳多少kg?
(2)若将100kg这种鸡蛋壳加工成钙片,则能加工成每片含钙量为0.4g的钙片多少片?
(1)可产生二氧化碳多少kg?
(2)若将100kg这种鸡蛋壳加工成钙片,则能加工成每片含钙量为0.4g的钙片多少片?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据碳酸钙的质量结合反应的化学方程式可以计算出二氧化碳的质量;
(2)根据碳酸钙的质量结合碳酸钙中钙元素的质量分数可以完成解答.
(2)根据碳酸钙的质量结合碳酸钙中钙元素的质量分数可以完成解答.
解答:解:(1)100kg鸡蛋壳中碳酸钙的质量为:100kg×50%=50kg
设生成二氧化碳的质量为x
CaCO3
CaO+CO2↑
100 44
50kg x
=
解得:x=22kg
(2)100kg这种鸡蛋壳中含钙的质量为:100kg×50%×
×100%=20kg=20000g
所以可以加工成钙片的:20000g÷0.4g/片=50000片
答:(1)可产生二氧化碳22kg;
(2)若将100kg这种鸡蛋壳加工成钙片,则能加工成每片含钙量为0.4g的钙片50000片.
设生成二氧化碳的质量为x
CaCO3
| ||
100 44
50kg x
| 100 |
| 50kg |
| 44 |
| x |
解得:x=22kg
(2)100kg这种鸡蛋壳中含钙的质量为:100kg×50%×
| 40 |
| 40+12+16×4 |
所以可以加工成钙片的:20000g÷0.4g/片=50000片
答:(1)可产生二氧化碳22kg;
(2)若将100kg这种鸡蛋壳加工成钙片,则能加工成每片含钙量为0.4g的钙片50000片.
点评:解答本题可用数据分析法,即解题时正确分析数据,找出数据的变化特征及彼此之间的关系,将综合复杂的问题分解为简单的计算,从而顺利解题.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
绿色化学的核心是要利用化学原理从源头上减少和消除工业生产对环境的污染.寻找可以充分利用的、无毒害的原材料和能源,且在各个环节都能实行洁净、无污染的反应途径和工艺,是现代化学工业追求的目标.下列做法不符合这一理念的是( )
| A、用可降解塑料取代聚乙烯等塑料制品 | ||
| B、禁止汽车使用含铅汽油 | ||
| C、用太阳能发电代替燃煤发电 | ||
D、铜+浓硫酸
|

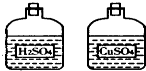 某同学用化学方法除掉一包铜、铁混合物中的铁,在实验台上有两瓶溶液(如图),从其中一瓶中取出100g溶液倒入烧杯中,他将该包混合物投入装有该溶液的烧杯中,恰好完全反应后过滤,得滤渣8.8克和溶液110.8克,求混合物中铁的质量分数.
某同学用化学方法除掉一包铜、铁混合物中的铁,在实验台上有两瓶溶液(如图),从其中一瓶中取出100g溶液倒入烧杯中,他将该包混合物投入装有该溶液的烧杯中,恰好完全反应后过滤,得滤渣8.8克和溶液110.8克,求混合物中铁的质量分数.