题目内容
有一包白色粉末,它可能是碳酸钙、氢氧化钙或两种物质的混合物.同学们设计了以下四种实验方案并得出相应的结论.其中方案都可行的是( )
方案1:取样品加入试管中,滴加稀盐酸,有气泡产生,则白色粉末是碳酸钙.
方案2:取样品加入试管中,滴加稀盐酸,无气泡产生,则白色粉末是氢氧化钙.
方案3:取样品加入试管中,加水振荡,静置,下层有不溶物,上层清液中滴入酚酞溶液,溶液变红,则白色粉末是碳酸钙和氢氧化钙的混合物.
方案4:取样品加入试管中,加水振荡,静置过滤.取滤液滴入酚酞溶液,溶液变红;再取滤渣加入稀盐酸,有气泡产生,则白色粉末是碳酸钙和氢氧化钙的混合物.
方案1:取样品加入试管中,滴加稀盐酸,有气泡产生,则白色粉末是碳酸钙.
方案2:取样品加入试管中,滴加稀盐酸,无气泡产生,则白色粉末是氢氧化钙.
方案3:取样品加入试管中,加水振荡,静置,下层有不溶物,上层清液中滴入酚酞溶液,溶液变红,则白色粉末是碳酸钙和氢氧化钙的混合物.
方案4:取样品加入试管中,加水振荡,静置过滤.取滤液滴入酚酞溶液,溶液变红;再取滤渣加入稀盐酸,有气泡产生,则白色粉末是碳酸钙和氢氧化钙的混合物.
| A、方案1和方案2 |
| B、方案2和方案4 |
| C、方案3和方案4 |
| D、方案1和方案3 |
考点:化学实验方案设计与评价,碱的化学性质,盐的化学性质
专题:简单实验方案的设计与评价
分析:氢氧化钙微溶于水,水溶液呈碱性,能使酚酞试液变红,而碳酸钙不溶于水,能与盐酸反应生成二氧化碳气体;根据现象对结论作出评价;要证明只含有其中一种成分,在设计实验时要能排除另一种物质的存在;要证明二者均有,要利用氢氧化钙和碳酸钙的性质进行设计.
解答:解:方案1:碳酸钙或碳酸钙与氢氧化钙的混合物滴加盐酸都会产生二氧化碳气体,所以方案1都不正确;
方案2:取样品加入试管中,滴加稀盐酸,无气泡产生,说明没有碳酸钙,故白色粉末是氢氧化钙,所以方案2都正确;
方案3:氢氧化钙微溶于水,会形成沉淀,故氢氧化钙或氢氧化钙与碳酸钙的混合物与水混合都能形成沉淀,所以方案3不正确;
方案4:取样品加入试管中,加水振荡,静置过滤.取滤液滴入酚酞溶液,溶液变红,说明溶液呈碱性,所以一定含有氢氧化钙;再取滤渣加入稀盐酸,有气泡产生,说明一定含有碳酸钙,则白色粉末是碳酸钙和氢氧化钙的混合物,所以方案4正确.
故选:B.
方案2:取样品加入试管中,滴加稀盐酸,无气泡产生,说明没有碳酸钙,故白色粉末是氢氧化钙,所以方案2都正确;
方案3:氢氧化钙微溶于水,会形成沉淀,故氢氧化钙或氢氧化钙与碳酸钙的混合物与水混合都能形成沉淀,所以方案3不正确;
方案4:取样品加入试管中,加水振荡,静置过滤.取滤液滴入酚酞溶液,溶液变红,说明溶液呈碱性,所以一定含有氢氧化钙;再取滤渣加入稀盐酸,有气泡产生,说明一定含有碳酸钙,则白色粉末是碳酸钙和氢氧化钙的混合物,所以方案4正确.
故选:B.
点评:本考点属于实验探究题,主要考查了氢氧化钙和碳酸钙的化学性质,通过对实验方案的设计和评价,能够培养学生的实验能力,养成对实验进行评价我自我设计实验的习惯.

练习册系列答案
相关题目
2013年诺贝尔化学奖获得者三位美国化学家利用计算机载体,将传统的化学实验搬进网络世界.下列化学实验基本操作中正确的是( )
A、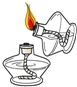 点燃酒精灯 |
B、 取用颗粒状固体 |
C、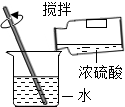 稀释浓硫酸 稀释浓硫酸 |
D、 测定溶液的pH |
某工厂甲乙两车间,排放出来的污水中分别含有大量的Ag+、Ba2+、Fe3+、Na+、Cl-、(SO4)2-、NO3-、OH-.经检验,甲车间污水pH值>7,乙车间污水中含有的离子可能是( )
| A、Ag+、Fe3+、Na+、(NO3)- |
| B、Ag+、Fe3+、(NO3)-、Ba2+ |
| C、Ag+、Fe3+、(NO3)-、(SO4)2- |
| D、Na+、OH-、Cl-、(SO4)2- |
下列物质中不属于盐的是( )
| A、洗涤用的纯碱 |
| B、消毒用的高锰酸钾 |
| C、医疗上做钡餐透视用的硫酸钡(BaSO4) |
| D、食用蔗糖(C12H22O11) |
下列有关催化剂的叙述正确的是( )
| A、催化剂能改变其他物质化学反应的速率 |
| B、催化剂能加快一切物质化学反应的速率 |
| C、有些化学反应,没有催化剂就不能发生 |
| D、催化剂并没有参与化学反应,所以化学反应不需要催化剂 |
能够说明镁条在空气中的燃烧属于化学变化的根本依据是( )
| A、发出耀眼的强光 |
| B、生成白色固体 |
| C、镁条迅速变短 |
| D、放出大量的热 |
科学探究有许多环节,其中第一步是( )
| A、提出问题 | B、收集证据 |
| C、交流反思 | D、获得结论 |