题目内容
8.将一定量的碳酸钠和碳酸氢钠的固体混合物与足量的稀盐酸反应,得到气体4.4g.则该固体混合物的质量可能是( )| A. | 10.6 g | B. | 9 g | C. | 8.4 g | D. | 4.2 g |
分析 利用极限法,假设固体全是碳酸钠或碳酸氢钠,根据二氧化碳的质量求出碳酸钠或碳酸氢钠的质量,则该固体混合物的质量介于二者之间.
解答 解:假设固体全是碳酸钠,设碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{44}=\frac{x}{4.4g}$
x=10.6g
假设固体全是碳酸氢钠,设碳酸氢钠的质量为y
NaHCO3+HCl=NaCl+H2O+CO2↑
84 44
y 4.4g
$\frac{84}{44}=\frac{y}{4.4g}$
y=8.4g
故该固体混合物的质量介于二者之间.
故选B.
点评 采用假设法解决此题是解题关键.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
18.金属的活动性顺序由强到弱排列的是( )
| A. | Mg Fe Zn | B. | Cu Hg Ag | C. | Na Ca K | D. | Zn Al Fe |
19.古语道“人要实,火要虚”,其中“火要虚”的意思是说:燃烧木柴时,要尽量架空些,这样才能燃烧得更旺.“火要虚”的实质是( )
| A. | 散热的速度加快 | B. | 增大木柴与空气的接触面积 | ||
| C. | 木柴的着火点降低 | D. | 提高空气中氧气的含量 |
16.下列对质量守恒定律的认识错误的是( )
| A. | 研究的是化学变化前后物质总质量的变化而不是物理变化 | |
| B. | 从宏观上看参与反应的所有反应物的总质量等于生成物的总质量 | |
| C. | 从微观上看原子的种类、数目、质量都保持不变 | |
| D. | 化学反应前后元素的质量、分子的数目可能会改变 |
13.在一个密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,则关于此反应认识错误的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 20 | 2 | 1 | 37 |
| 反应后质量(g) | 未测 | 32 | 1 | 12 |
| A. | 物质Z一定是该反应的催化剂 | B. | 反应后物质X的质量为15g | ||
| C. | 反应中Y、Q的质量比为6:5 | D. | 物质Y一定是化合物 |
20.如图是某化学反应的微观示意图,相同的球代表同种原子.下列说法正确的是( )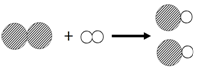
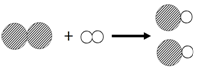
| A. | 两种反应物均为化合物 | B. | 该反应属于分解反应 | ||
| C. | 分子在化学反应中可以再分 | D. | 分子在化学反应中不可再分 |
17.枯燥的阿拉伯数字在化学世界里表示着不同含义,下列符号中数字“2”表示的意义正确的是( )
| A. | Mg2+:镁的化合价 | |
| B. | $\stackrel{+2}{CaO}$:钙离子带两个单位正电荷 | |
| C. | 2H:元素个数 | |
| D. | CO2:一个二氧化碳分子中氧原子个数 |
18.下列实验中,能达到相应目的是( )
| A. | 分离CaSO4和CaCl2固体:取样,加足量水溶解,过滤 | |
| B. | 制备Fe(OH)3:将Fe2(SO4)3溶液和适量的Ba(OH)2溶液混合,过滤 | |
| C. | 除去CO2中的HCl气体和水蒸气:将混合气体依次通过NaOH溶液、浓硫酸 | |
| D. | 鉴别稀盐酸、NaOH和NaCl三种溶液:取样,分别滴入酚酞溶液后再相互混合 |