题目内容
19. 如图是测定空气中氧含量的装置图,结合图示探究有关问题.
如图是测定空气中氧含量的装置图,结合图示探究有关问题.(1)试管口为什么要略向下倾斜?
(2)根据表提供的数据,完成表.
| 硬质玻璃管的容积 | 反应前注射器中气体体积 | 反应后注射器中气体体积 | 反应消耗的氧气的体积 |
| 18mL | 7mL |
分析 本题是测定空气中氧气的含量,因为铜加热生成氧化铜,几乎不占空间,使容器内的气体减少,注射器内气体减少的量就是氧气的量,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应;从两种装置的区别来分析评价装置;根据测定空气中氧气的体积分数实验的原理、注意事项分析回答误差原因.
解答 解:(1)为防止泠凝水倒流将试管炸裂,试管口要略向下倾斜;
(2)注射器内气体减少的量就是氧气的体积,氧气约占空气体积的$\frac{1}{5}$,则实验测得空气中氧气的体为:(18ml+7mL)×$\frac{1}{5}$=5mL,反应后注射器中气体体积7mL-5mL=2mL.
(3)在实验加热过程中,为使空气中的氧气充分反应,应交替缓慢推动两个注射器活塞;故答案为:使空气中氧气与铜粉充分反应;
答案:
(1)为防止泠凝水倒流将试管炸裂;
(2)2mL;5mL.
(3)使空气中氧气与铜粉充分反应.
点评 本考点是用铜粉测定氧气在空气中的体积分数,属于实验方法和过程的探究,注重了实验方案的评价,对实验方案进行评价是近几年中考的一个重点.评价包括对实验方案的评价、实验过程的评价、实验结论的评价等,要认真把握.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
9.“化学氧自救呼吸器”中的超氧化钾(K02)是一种白色粉末,它能与佩戴者呼出气体中 的水蒸气和二氧化碳发生化学反应,产生氧气并放出热量,下列说法不正确的是
( )
( )
| A. | KO2应密封保存 | |
| B. | 呼吸器充分利用了呼出气体中的二氧化碳和水蒸气 | |
| C. | 呼吸器可用于矿山井下的防护自救 | |
| D. | 自救者用此呼吸器可以吸入到纯净的氧气 |
7.有X Y Z三种金属,若把X和Y放入稀硫酸中,Y溶解并产生氢气,X不反应,若把X和Z放入硝酸银溶液中,过一会儿,X表面有银析出,而Z没有变化.根据以上事实,判断三种金属活动性由强到弱的顺序( )
| A. | Z Y X | B. | X Y Z | C. | Y X Z | D. | X Z Y |
14.下表是生活中一些物质的PH
有关它的说法正确的是( )
| 物质种类 | 厕所清洁剂 | 橘子汁 | 牛奶 | 草木灰水 | 厨房清洁剂 |
| PH | 1 | 3 | 6.5 | 11 | 12.5 |
| A. | 草木灰可改良碱性土壤 | B. | 橘子汁能使酚酞试液变红 | ||
| C. | 牛奶酸性比橘子强 | D. | 胃酸过多的人不易多吃橘子 |
18. 如图所示是实验中某项净化水的操作,则此操作应用的净水方法是( )
如图所示是实验中某项净化水的操作,则此操作应用的净水方法是( )
 如图所示是实验中某项净化水的操作,则此操作应用的净水方法是( )
如图所示是实验中某项净化水的操作,则此操作应用的净水方法是( )| A. | 沉淀法 | B. | 过滤法 | C. | 蒸馏法 | D. | 结晶法 |
19.对比分析是化学研究和学校的基本方法,为了验证化学反应是否遵守质量守恒定律,甲、乙、冰三个兴趣小组的同学分别设计了如图所示的实验.
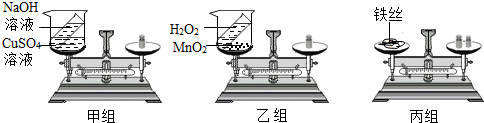
【实验步骤】如图所示,甲、乙两组同学分别把盛有适量NaOH、H2O2溶液的小试管放入盛有CuSO4溶液、MnO2溶液的烧杯中,并将烧杯放到天平上调至平衡,接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡,丙组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上,用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却后将所得的物质与石棉网一起再放回托盘天平上称量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
(2)通过对上述实验的对比分析,甲丙两组同学发现乙同学的结论是正确的,但结论却是错误的.在实验操作完全正确的情况下,请分析导致乙组实验实验反应后天平不平衡的原因是反应生成的氧气逸散到空气中,质量减少.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】从微观角度分析化学反应遵守质量守恒定律的原因是:化学反应前后,原子的质量、种类、数目均不变.

【实验步骤】如图所示,甲、乙两组同学分别把盛有适量NaOH、H2O2溶液的小试管放入盛有CuSO4溶液、MnO2溶液的烧杯中,并将烧杯放到天平上调至平衡,接着取下烧杯并将其倾斜,使物质混合发生反应,待反应后再把烧杯放到天平上,观察天平是否平衡,丙组同学取一根打磨干净的细铁丝和一个石棉网,将它们一起放在托盘天平上,用砝码平衡,取下铁丝,将铁丝放在充满氧气的集气瓶中点燃,燃烧结束并冷却后将所得的物质与石棉网一起再放回托盘天平上称量.
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | 化学方程式 | 结论 | |
| 甲组 | 产生蓝色沉淀,天平①平衡(填“平衡”或“不平衡”) | ②2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 | 该反应遵守质量守恒定律 |
| 乙组 | 烧杯中产生大量气泡,天平不平衡 | ③2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | 该反应不遵守质量守恒定律 |
| 丙组 | ④剧烈燃烧,火星四射,生成黑色固体,反应前后称量质量不相等 | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | 该实验遵守质量守恒定律 |
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】从微观角度分析化学反应遵守质量守恒定律的原因是:化学反应前后,原子的质量、种类、数目均不变.

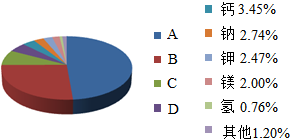 从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料.请回答-下列问题:
从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料.请回答-下列问题: