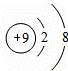题目内容
1小题,共10分)
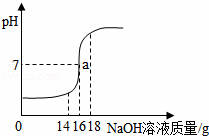
将5%的NaOH溶液逐滴加入到10g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.边回答:
(1)a点溶液中大量存在的离子有 ;
(2)当恰好完全反应时,消耗NaOH溶液的质量为 ;
(3)计算稀盐酸中溶质的质量分数.
| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | a点时,溶液的pH等于7,说明稀盐酸和氢氧化钠恰好完全反应生成氯化钠和水,溶液中大量存在的离子是钠离子和氯离子; 根据图中信息可以判断当恰好完全反应时,消耗NaOH溶液的质量; 根据氢氧化钠溶液质量、溶质质量分数可以计算氯化氢的质量,进一步可以计算稀盐酸中溶质的质量分数. |
| 解答: | 解:(1)a点溶液中大量存在的离子有钠离子和氯离子. 故填:钠离子和氯离子. (2)当恰好完全反应时,消耗NaOH溶液的质量为16g. 故填:16g. (3)设稀盐酸中氯化氢的质量为x, NaOH+HCl═NaCl+H2O, 40 36.5 16g×5% x
x=0.73g, 稀盐酸中溶质的质量分数为: 答:稀盐酸中溶质的质量分数为7.3%. |
| 点评: | 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性. |

锡)下列归纳和总结完全正确的一组是( )
| A.对除杂的认识 | B.食品安全 |
| ①用稀硫酸出去Zn中混有的Ag ②用灼烧的方法出去Fe2O3中混有的C ③用碳酸钙出去CaCl2溶液中的HCl | ①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③补充维生素A防止夜盲症 |
| C.对现象的认识 | D.化学学科的价值 |
| ①花香四溢,说明分子在不断运动 ②红磷燃烧,有大量白雾产生 ③电解水生成氢气和氧气的体积比为2:1 | ①研制高效低毒农药,保障粮食生产 ②开发新型材料,改善人类生存条件 ③利用化学合成药物,保障人体健康 |
|
| A. | A | B. | B | C. | C | D. | D |
氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
|
| A. | 都能与指示剂作用 | B. | 都能解离出氢氧根离子 |
|
| C. | 都能解离出金属阳离子 | D. | 都含有氢元素和氧元素 |
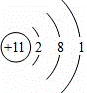
下列对微粒的描述中,不正确的是( )
|
| A. |
易失电子 | B. |
易形成阴离子 | C. |
阳离子 | D. |
化学性质稳定 |
为除去下列物质中的杂质(括号内为杂质),相应的操作方法不能达到目的是:( )
| 选项 | 物质(杂质) | 操作方法 |
| A | CO(CO2) | 将气体通过足量的NaOH溶液后干燥 |
| B | CuO(Cu) | 通入足量氧气气体加热 |
| C | Na2SO4溶液(NaHCO3) | 加入稀盐酸至不再产生气泡为止 |
| D | FeSO4溶液(CuSO4) | 加入过量的铁屑充分反应后过滤 |
|
| A. | A | B. | B | C. | C | D. | D |
 =
=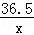 ,
, ×100%=7.3%,
×100%=7.3%, _________,包括事例为(2)__________(填序号)。
_________,包括事例为(2)__________(填序号)。