题目内容
16.有一包白色粉末,可能是Mg(OH)2、CaCO3、FeCl3、BaCl2、Na2SO4、KOH中的一种或几种,为检验其组成,进行如下实验:(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是Mg(OH)2、CaCO3、BaSO4,原混合物中一定不含有FeCl3.
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体,则原混合物中一定含有CaCO3,写出该反应方程式CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生;将其导出后的气体再通入另一份滤液中,立即产生白色沉淀,再过滤.出现上述现象的原因是实验(2)中产生的气体里含有氯化氢气体.
(4)由上述(1)(2)(3)可知,原混合物中一定有 的物质是CaCO3、BaCl2、KOH.
分析 本题属于推断题,根据题目给出的信息:取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是Mg(OH)2、CaCO3、BaSO4,原混合物中一定不含有FeCl3,因为氯化铁溶液是黄色的;向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体,则原混合物中一定含有CaCO3,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;一定没有硫酸钡,即BaCl2、Na2SO4不能共存;将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生;将其导出后的气体再通入另一份滤液中,立即产生白色沉淀,再过滤.出现上述现象的原因是实验(2)中产生的气体里含有氯化氢气体;也因此得出一定有BaCl2、KOH;由上述(1)(2)(3)可知,原混合物中一定有 的物质是:CaCO3、BaCl2、KOH.
解答 解:(1)根据题目给出的信息:取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是Mg(OH)2、CaCO3、BaSO4,原混合物中一定不含有FeCl3,因为氯化铁溶液是黄色的;故答案为:Mg(OH)2、CaCO3、BaSO4;FeCl3;
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体,则原混合物中一定含有CaCO3,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;故答案为:CaCO3;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生;将其导出后的气体再通入另一份滤液中,立即产生白色沉淀,再过滤.出现上述现象的原因是实验(2)中产生的气体里含有氯化氢气体;故答案为:氯化氢气体;
(4)由上述(1)(2)(3)可知,原混合物中一定有 的物质是:CaCO3、BaCl2、KOH;故答案为:CaCO3、BaCl2、KOH;
点评 本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.本考点是中考的重要内容之一,一般有两种类型:一是图框式推断题;二是文字描述型推断题;本题属于第二种类型.不论哪一种类型,都是通过实验现象,从而得出物质的组成.此考点主要出现在填空题和实验题中.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 常见的三种强酸:盐酸,硫酸,硝酸 | |
| B. | 浓硫酸的三个特性:吸水性,脱水性,腐蚀性 | |
| C. | 氢氧化钠的三个俗称:纯碱,烧碱,苛性钠 | |
| D. | 遇水放热的三种物质:浓硫酸,氢氧化钠,生石灰 |
| A. |  碳酸钙固体 | B. |  氢氧化钠溶液 | C. |  氢气 | D. |  稀盐酸溶液 |
 根据如图的实验装置图回答问题.
根据如图的实验装置图回答问题.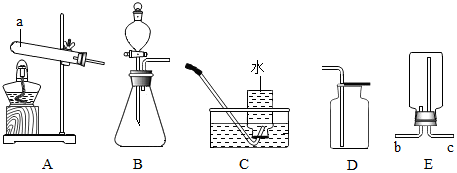
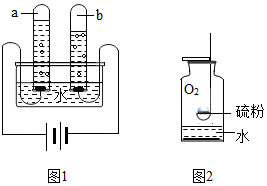 水与人类的生活和生产密切相关,请回答下列问题:
水与人类的生活和生产密切相关,请回答下列问题: