题目内容
如图是毛星棋同学配制100g溶质质量分数为10%的NaCl溶液的实验操作示意图:
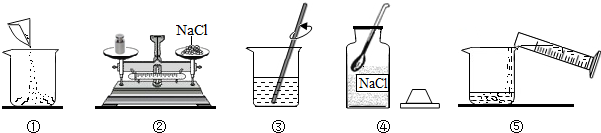
(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和 ;
(2)指出图中的一处错误操作 ;配制时应选择 (10mL或50mL或100mL)的量筒量取所需要的水;用上述图示的序号表示配制溶液的操作顺序 ;会导致配制结果比10%小,则可能的原因是 (填字母).
A.配溶液时仰视量水 B.过滤时待滤液面高于滤纸边缘 C.砝码与称量物倒置 D.砝码锈蚀.

(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和
(2)指出图中的一处错误操作
A.配溶液时仰视量水 B.过滤时待滤液面高于滤纸边缘 C.砝码与称量物倒置 D.砝码锈蚀.
考点:一定溶质质量分数的溶液的配制,称量器-托盘天平
专题:溶液、浊液与溶解度
分析:(1)根据实验操作示意图中所涉及的玻璃仪器进行分析解答.
(2)托盘天平的使用要遵循“左物右码”的原则;利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量,进而确定量筒的量程.
根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
溶质质量分数偏小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答.
(2)托盘天平的使用要遵循“左物右码”的原则;利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量,进而确定量筒的量程.
根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
溶质质量分数偏小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答.
解答:解:(1)图中的玻璃仪器分别是广口瓶、量筒、烧杯和玻璃棒.
(2)托盘天平的使用要遵循“左物右码”的原则,图中称量时药品与砝码的位置放反了.
溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为10%的NaCl溶液,需氯化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-10g=90g(合90mL);选取量筒时,尽量选用能一次量取的最小规格的量筒.用量筒量取90mL水,应选择100mL的量筒.
配制100g溶质质量分数为10%的NaCl溶液的步骤:计算、称量(量取)、溶解、装瓶贴签,用图示的序号表示为:④②①⑤③.
A.配溶液时仰视量水,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数小于10%.
B.配制溶液时,无需过滤,过滤时待滤液面高于滤纸边缘,不影响溶质质量分数的大小.
C.砝码与称量物倒置,会造成实际所取的溶质的质量偏小,则使溶质质量分数小于10%.
D.砝码锈蚀,会造成实际所取的溶质的质量偏小,则使溶质质量分数小于10%.
故答案为:(1)玻璃棒;(2)称量时药品与砝码的位置放反了;100mL;④②①⑤③;ACD.
(2)托盘天平的使用要遵循“左物右码”的原则,图中称量时药品与砝码的位置放反了.
溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为10%的NaCl溶液,需氯化钠的质量=100g×10%=10g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-10g=90g(合90mL);选取量筒时,尽量选用能一次量取的最小规格的量筒.用量筒量取90mL水,应选择100mL的量筒.
配制100g溶质质量分数为10%的NaCl溶液的步骤:计算、称量(量取)、溶解、装瓶贴签,用图示的序号表示为:④②①⑤③.
A.配溶液时仰视量水,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数小于10%.
B.配制溶液时,无需过滤,过滤时待滤液面高于滤纸边缘,不影响溶质质量分数的大小.
C.砝码与称量物倒置,会造成实际所取的溶质的质量偏小,则使溶质质量分数小于10%.
D.砝码锈蚀,会造成实际所取的溶质的质量偏小,则使溶质质量分数小于10%.
故答案为:(1)玻璃棒;(2)称量时药品与砝码的位置放反了;100mL;④②①⑤③;ACD.
点评:本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、注意事项、所需仪器等是正确解答本题的关键.

练习册系列答案
相关题目

