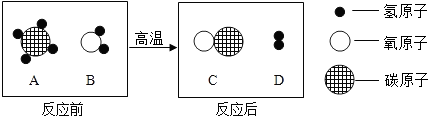
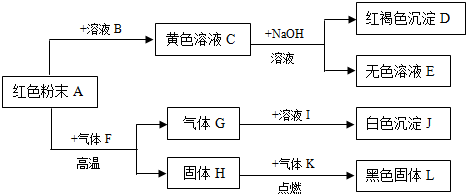
题目内容
5.已知Na2CO3样品中含有少量的NaCl杂质,化学兴趣小组为测定Na2CO3样品的纯度,设计如下实验: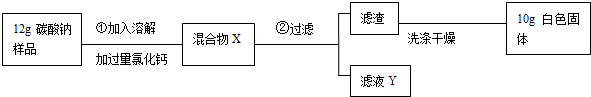
(1)在①步操作中观察到的现象有白色沉淀生成加入过量CaCl2溶液的目的是除净碳酸钠.
(2)滤液Y中的溶质是氯化钠和氯化钙.
(3)若过程①所加氯化钙溶液的量不足,则计算出碳酸钠样品的纯度将偏小(填偏大、偏小、不受影响).
(4)根据实验数据计算样品中碳酸钠的质量(保留一位小数).
分析 根据题目给出的流程图和信息:当加入过量的氯化钙溶液时,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,因此滤渣是碳酸钙,滤液Y中的溶质是氯化钠和氯化钙;若过程①所加氯化钙溶液的量不足,则计算出的碳酸钠样品的纯度将偏小,因为碳酸钠会有剩余;根据白色固体碳酸钙是10g,可以求出碳酸钠的质量,然后根据质量分数公式求碳酸钠的质量分数.
解答 解:
(1)当加入过量的氯化钙溶液时,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,故答案为:有白色沉淀生成;加入过量CaCl2溶液的目的是除净碳酸钠;
(2)当加入过量的氯化钙溶液时,碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,因此滤液Y中的溶质是氯化钠和氯化钙,故答案为:氯化钠和氯化钙
(3)若过程①所加氯化钙溶液的量不足,则计算出的碳酸钠样品的纯度将偏小,因为碳酸钠会有剩余故答案为:偏小
(4)设碳酸钠的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 10g
$\frac{106}{x}=\frac{100}{10g}$
x=10.6g
碳酸钠的质量是10.6g.
答案:
(1)有白色沉淀生成;除净碳酸钠;
(2)氯化钠和氯化钙;
(3)偏小;
(4)样品中碳酸钠的质量为10.6g.
点评 本题属于实验探究题,有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;有关的计算要准确,本考点主要出现在填空题和实验题中.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
20.下列净水方法中,对水的净化程度相对较高的是( )
| A. | 过滤 | B. | 蒸馏 | C. | 吸附沉淀 | D. | 静置沉淀 |
18.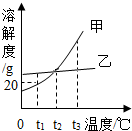 根据如图的溶解度曲线,判断下列说法不正确的是( )
根据如图的溶解度曲线,判断下列说法不正确的是( )
 根据如图的溶解度曲线,判断下列说法不正确的是( )
根据如图的溶解度曲线,判断下列说法不正确的是( )| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | t1℃时,甲的饱和溶液中溶质和溶剂的质量比为1:5 | |
| C. | t2℃时,甲、乙两物质的溶解度相等 | |
| D. | 将t3℃时甲、乙两物质的饱和溶液降温到t1℃,甲析出的晶体多 |
17.下列说法中错误的是( )
| A. | 水银是由汞原子直接构成的 | |
| B. | 液态氧、氧气、固态氧都是由氧元素组成的同一种单质 | |
| C. | 二氧化碳是由2个氧元素和1个碳元素组成的 | |
| D. | 一个二氧化碳分子由2个氧原子和1个碳原子构成 |
15.松花蛋,又称皮蛋、卞蛋.其中一种加工工艺的主要原料配方为:鸭蛋10Kg,水10Kg,生石灰1.2Kg,纯碱0.53Kg,食盐0.35Kg.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是氧化钙与水反应能放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质:甲同学推断只有Ca(OH)2,乙同学推断只有Na2CO3,丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
【探究结论】甲同学的推断是正确的.
【知识应用】①皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是酸碱起中和反应.
②料液中起主要作用的是烧碱.现行配方中,直接用烧碱代替石灰和纯碱作用生成的烧碱.若加工10Kg的鸭蛋,需要烧碱的质量是多少千克?(请写出计算过程)
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是氧化钙与水反应能放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【交流讨论】①一定含有NaOH、NaCl
②可能还含有其它溶质:甲同学推断只有Ca(OH)2,乙同学推断只有Na2CO3,丙同学推断有Ca(OH)2、也有Na2CO3
通过进一步讨论,大家一致认为丙同学的推断是错误的,理由是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(用化学方程式表示).
【实验探究】
| 实验步骤 | 实验现象 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 |
| 另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
【知识应用】①皮蛋食用时加入一些食醋,可以去除氨味和涩感,原因是酸碱起中和反应.
②料液中起主要作用的是烧碱.现行配方中,直接用烧碱代替石灰和纯碱作用生成的烧碱.若加工10Kg的鸭蛋,需要烧碱的质量是多少千克?(请写出计算过程)