题目内容
9.废旧金属可以回收利用,用合金废料(含Fe、Cu和Al)制取FeSO4和CuSO4溶液的实验流程如图(部分生成物已略):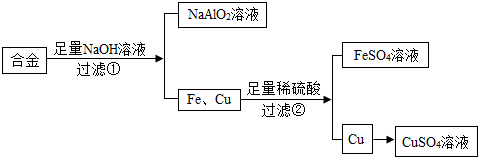
(1)合金属于混合物(填“纯净物”或“混合物”);
(2)步骤①反应的化学方程式为:2Al+2NaOH+2R═2NaAlO2+3H2↑,依据质量守恒定律推出R的化学式为H2O,步骤②反应的化学方程式为Fe+H2SO4=FeSO4+H2↑;
(3)由Cu制取CuSO4溶液有以下三种途径:
I.Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O
Ⅱ.2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO CuO+H2SO4═CuSO4+H2O
Ⅲ.3Cu+8HNO3═3Cu(NO3)+2NO↑+4H2O
你认为最佳途径是Ⅱ(填序号),理由是不会生成有毒气体二氧化硫,生成相同质量的硫酸铜,消耗的硫酸少.
分析 (1)根据合金的定义和混合物的定义进行分析;
(2)根据化学反应前后原子个数不变,铁和稀硫酸反应生成硫酸亚铁和氢气进行分析;
(3)根据制取硫酸铜的三种途径中需要的反应物以及生成物进行分析.
解答 解:(1)合金是金属和金属,金属和非金属经过熔合得到的,混合物是由两种或多种物质组成的,所以合金属于混合物;
(2)生成物中有2个钠原子,2个铝原子,4个氧原子,6个氢原子,反应物中有2个铝原子,2个钠原子、氢原子、氧原子,所以R是H2O;
铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(3)通过分析各种途径中的反应物和生成物可知,最佳途径是Ⅱ,理由是:不会生成有毒气体二氧化硫,生成相同质量的硫酸铜,消耗的硫酸少.
故答案为:(1)混合物;
(2)H2O;Fe+H2SO4=FeSO4+H2↑;
(3)Ⅱ,不会生成有毒气体二氧化硫,生成相同质量的硫酸铜,消耗的硫酸少.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识进行解答.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
19.下列实验的操作如图所示,其中正确的是( )
| A. |  读取液体体积 | B. |  称量固体烧碱 | C. | 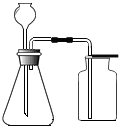 Zn和稀H2SO4制H2 | D. | 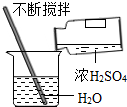 稀释浓硫酸 |
17.下列物质的化学式和俗名对应不相符的是( )
| A. | Hg-水银 | B. | NaHCO3-苏打 | C. | NaOH-苛性钠 | D. | C2H5OH-酒精 |
4.下列实验方案合理的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 实验室制取CO2 | 块状大理石与稀硫酸 |
| B | 鉴别硬水和软水 | 观察液体是否浑浊 |
| C | 鉴别H2O、KCl溶液 | AgNO3溶液 |
| D | 除去CO2中少量的CO | 通入O2,点燃 |
| A. | A | B. | B | C. | C | D. | D |
14.下列描述中表达的是物质化学性质的是( )
| A. | 干冰能升华 | B. | 氧气是一种无色无味的气体 | ||
| C. | 氢氧化钠在空气中易变质 | D. | 水蒸发产生水蒸气 |
1.检验氢气纯度时,判断氢气较纯的现象是( )
| A. | 听到尖锐的爆鸣声 | B. | 听到轻微的爆鸣声 | ||
| C. | 未听到声音 | D. | 试管炸裂 |
18.下列物质中所含氮元素化合价最低的是( )
| A. | NO2 | B. | N2 | C. | NH4Cl | D. | HNO3 |
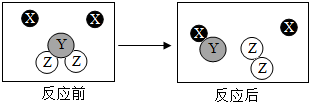 走进化学变化的微观世界,有利于进一步认识化学变化.如图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,据图回答问题;
走进化学变化的微观世界,有利于进一步认识化学变化.如图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,据图回答问题;