题目内容
某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖.对于该溶液是否变质,同学们提出如下猜想:
猜想一:没有变质,溶质是NaOH
猜想二:部分变质,溶质是
猜想三:全部变质,溶质是Na2CO3
有同学进行了以下探究:

(1)请完成下表(已知CaCl2溶液呈中性)
(2)实验探究结果:该溶液部分变质.因此,实验取完药品后应 .
(3)实验反思:实验方案步骤(1)中CaCl2溶液能否改为Ca(OH)2溶液? (填“能”或“不能”),理由是 .
猜想一:没有变质,溶质是NaOH
猜想二:部分变质,溶质是
猜想三:全部变质,溶质是Na2CO3
有同学进行了以下探究:

(1)请完成下表(已知CaCl2溶液呈中性)
| 假设和现象 | 判断和化学方程式 | |
| a | 若现象Ⅰ无白色沉淀产生,现象Ⅱ溶液变红色 | 则该样品中溶质是 |
| b | 若现象Ⅰ有白色沉淀产生,现象Ⅱ溶液变红色 | 则该样品中溶质是 |
| c | 若现象Ⅰ有白色沉淀产生,现象Ⅱ溶液不变色 | 则该样品中溶质是 |
(3)实验反思:实验方案步骤(1)中CaCl2溶液能否改为Ca(OH)2溶液?
考点:药品是否变质的探究,碱的化学性质,盐的化学性质
专题:科学探究
分析:【提出假设】根据氢氧化钠易吸收空气中的二氧化碳来解答;
【设计实验】根据实验的现象结合氢氧化钠和碳酸钠的性质分析;
【实验探究结果拓展】该溶液部分变质,实验取完药品后应盖瓶盖;
【实验反思】如用氢氧化钙溶液代替氯化钙溶液,氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定原溶液是否有氢氧化钠;
【设计实验】根据实验的现象结合氢氧化钠和碳酸钠的性质分析;
【实验探究结果拓展】该溶液部分变质,实验取完药品后应盖瓶盖;
【实验反思】如用氢氧化钙溶液代替氯化钙溶液,氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定原溶液是否有氢氧化钠;
解答:解:【提出假设】氢氧化钠溶液易吸收空气中的二氧化碳生成碳酸钠而变质;若没有变质,溶质是NaOH;
若部分变质,则溶质是氢氧化钠和碳酸钠,化学式为:NaOH、Na2CO3;全部变质,溶质是Na2CO3;(1)【设计实验】有同学进行了以下探究:

完成下表(已知CaCl2溶液呈中性)
(2)【实验探究结果拓展】该溶液部分变质,因此,实验取完药品后应盖瓶盖;
(3)【实验反思】如用氢氧化钙溶液代替氯化钙溶液是不行的,因为氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定氢氧化钠的存在,也得不出氢氧化钠部分变质的结论;
故答案为:NaOH和Na2CO3;
(1)氢氧化钠;氢氧化钠和碳酸钠;CaCl2+Na2CO3=CaCO3↓+2NaCl;碳酸钠;
(2)盖瓶盖
(3)氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定原溶液是否含有氢氧化钠;
若部分变质,则溶质是氢氧化钠和碳酸钠,化学式为:NaOH、Na2CO3;全部变质,溶质是Na2CO3;(1)【设计实验】有同学进行了以下探究:

完成下表(已知CaCl2溶液呈中性)
| 假设和现象 | 判断和化学方程式 | |
| a | 若现象Ⅰ无白色沉淀产生,现象Ⅱ溶液变红色 | 则该样品中溶质是氢氧化钠 |
| b | 若现象Ⅰ有白色沉淀产生,现象Ⅱ溶液变红色 | 则该样品中溶质是氢氧化钠和碳酸钠.该反应化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl. |
| c | 若现象Ⅰ有白色沉淀产生,现象Ⅱ溶液不变色 | 则该样品中溶质是碳酸钠 |
(3)【实验反思】如用氢氧化钙溶液代替氯化钙溶液是不行的,因为氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定氢氧化钠的存在,也得不出氢氧化钠部分变质的结论;
故答案为:NaOH和Na2CO3;
(1)氢氧化钠;氢氧化钠和碳酸钠;CaCl2+Na2CO3=CaCO3↓+2NaCl;碳酸钠;
(2)盖瓶盖
(3)氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定原溶液是否含有氢氧化钠;
点评:此题是一道实验探究题,解题的关键是把握在证明氢氧化钠部分变质时,先除去氢氧化钠中的碳酸钠,然后再证明剩余溶液显碱性,才能说明氢氧化钠部分变质.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食易中毒.区别它们的一种方法是:将两者分别加热到320℃,没有明显现象的是食盐,能分解出一种具有刺激性气味气体的是亚硝酸钠,该气体可能是( )
| A、CO2 |
| B、SO2 |
| C、NO2 |
| D、HCl |
下列仪器名称,书写正确的是( )
| A、椎形瓶 | B、胶头滴管 |
| C、蒸发血 | D、长劲漏斗 |
目前,农村常用的化肥有:NH4HCO3、NH4NO3、KNO3、CO(NH2)2(尿素)、KH2PO4、KCl、Ca(H2PO4)2、NH4H2PO4等,下列化肥属于复合肥料的是( )
| A、NH4HCO3 |
| B、KNO3 |
| C、Ca(H2PO4)2 |
| D、NH4NO3 |
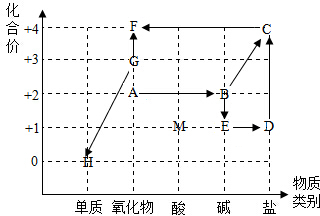 同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).已知A、H为固体,通常均可在食品包装袋中用于保存食品.人体胃酸中有大量M存在.A、B、C含有两种相同的元素.请回答下列问题:
同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).已知A、H为固体,通常均可在食品包装袋中用于保存食品.人体胃酸中有大量M存在.A、B、C含有两种相同的元素.请回答下列问题: