题目内容
15.向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入m g锌粉,充分反应后过滤,将滤渣洗涤,干燥后称量,质量仍为m g.据此,判断下列说法不正确的是( )| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀盐酸、一定有气泡产生 | |
| D. | 反应后的滤液中溶质可能是一种或两种 |
分析 锌比铁活泼,铁比银活泼,向一定质量的AgNO3和Fe(NO3)2的混合溶液中加入m g锌粉,锌先和硝酸银反应,如果硝酸银完全反应后锌有剩余,则锌再和硝酸亚铁反应.
解答 解:A、硝酸银、硝酸亚铁和锌反应的化学方程式及其质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,Zn+Fe(NO3)2=Zn(NO3)2+Fe,
65 216 65 56
由以上关系可知,锌和硝酸银反应时固体质量增加,锌和硝酸亚铁反应时固体质量减小,因此将滤渣洗涤,干燥后称量,质量仍为mg,说明硝酸银完全反应后,锌和硝酸亚铁发生了反应,滤渣中至少含有银和铁,该选项说法正确;
B、将滤渣洗涤,干燥后称量,质量仍为mg,说明硝酸银完全反应后,锌和硝酸亚铁发生了反应,因此取反应后的滤液滴加稀盐酸,无白色沉淀产生,该选项说法不正确;
C、将滤渣洗涤,干燥后称量,质量仍为mg,说明硝酸银完全反应后,锌和硝酸亚铁发生了反应,滤渣中至少含有银和铁,铁能和稀盐酸反应生成氯化亚铁和氢气,因此取滤渣滴加稀盐酸、一定有气泡产生,该选项说法正确;
D、当硝酸银、硝酸亚铁都完全和铁反应时,滤液中的溶质是硝酸锌,当硝酸银完全反应,硝酸亚铁部分反应时,滤液中的溶质是硝酸锌和硝酸亚铁,因此反应后的滤液中溶质可能是一种或两种,该选项说法正确.
故选:B.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
5.海洋是一个巨大的资源宝库,海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钠等.如图为综合利用海水制备金属镁的流程.

该流程中没有涉及到的化学反应是( )

该流程中没有涉及到的化学反应是( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
3. 赖氨酸是人体必需氨基酸之一,其化学式为C6H14N2O2,赖氨酸能促进人体发育、增强免疫功能等.下列有关叙述不正确的是( )
赖氨酸是人体必需氨基酸之一,其化学式为C6H14N2O2,赖氨酸能促进人体发育、增强免疫功能等.下列有关叙述不正确的是( )
 赖氨酸是人体必需氨基酸之一,其化学式为C6H14N2O2,赖氨酸能促进人体发育、增强免疫功能等.下列有关叙述不正确的是( )
赖氨酸是人体必需氨基酸之一,其化学式为C6H14N2O2,赖氨酸能促进人体发育、增强免疫功能等.下列有关叙述不正确的是( )| A. | 赖氨酸分子中碳、氧两种元素的原子个数比为3:1 | |
| B. | 赖氨酸属于有机化合物 | |
| C. | 赖氨酸中含有C、H、N、O四种原子 | |
| D. | 赖氨酸分子中含有24个原子核 |
20. 现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )
现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )
 现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )
现把足量的稀盐酸分为两等份,分别与等质量的X、Y金属反应,生成气体的质量与时间的关系如图所示.则下列说法错误的是( )| A. | 金属X、Y的活动性关系为:X>Y | |
| B. | t1时消耗稀盐酸的质量:X=Y | |
| C. | 若反应生成XCl2和YCl2,则X、Y的相对原子质量大小关系为:X<Y | |
| D. | t1时烧杯中溶液的质量:X<Y |
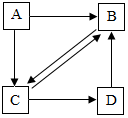 A、B、C、D都是初中化学常见的物质.它们之间的转化关系如图所示
A、B、C、D都是初中化学常见的物质.它们之间的转化关系如图所示 生活报2016年1月19日讯:目前,哈市范围内已发放回收箱近千个,先后有140个小区设置了旧衣回收箱,市民可就近捐赠衣物.据悉,所有捐赠的旧衣物均由黑龙江省慈善总会定时、定点回收.回收的旧衣物经过洗涤、消毒、熨烫、整理等专业处理后,全部用于帮助贫困家庭的救助.
生活报2016年1月19日讯:目前,哈市范围内已发放回收箱近千个,先后有140个小区设置了旧衣回收箱,市民可就近捐赠衣物.据悉,所有捐赠的旧衣物均由黑龙江省慈善总会定时、定点回收.回收的旧衣物经过洗涤、消毒、熨烫、整理等专业处理后,全部用于帮助贫困家庭的救助.
 能源、环境与入类社会密切相关.
能源、环境与入类社会密切相关.