题目内容
10.交警用装有重铬酸钾(K2Cr2O7)的检测仪,来检测司机是否酒后驾车,其原理是红色的重铬酸钾遇酒精后生成蓝绿色的物质.下列说法正确的是( )| A. | 重铬酸钾属于氧化物 | |
| B. | 重铬酸钾中钾元素与氧元素的质量比为2:7 | |
| C. | 重铬酸钾是由分子构成 | |
| D. | 重铬酸钾中铬元素的化合价为+6价 |
分析 A、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据重铬酸钾的微观构成,进行分析判断.
D、根据在化合物中正负化合价代数和为零,结合重铬酸钾的化学式进行解答即可.
解答 解:A、重铬酸钾是由钾、铬、氧三种元素组成的化合物,不属于氧化物,故选项说法错误.
B、重铬酸钾中钾元素与氧元素的质量比为(39×2):(16×7)≠2:7,故选项说法错误.
C、重铬酸钾是由钾离子和重铬酸根离子构成的,故选项说法错误.
D、钾元素显+1价,氧元素显-2价,设铬元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2x+(-2)×7=0,则x=+6价,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
18.2013年3月12日,西安市工商局抽检的15个批次炒货及坚果制品中,有一个批次的糖精钠(C7H5NO3S)含量不合格.糖精钠的甜度为蔗糖的几百倍,不易被人体代谢吸收,摄入后会在人体中长期存留、积累,影响人体健康.下列关于糖精钠的说法正确的是( )
| A. | 糖精钠共有5个原子 | B. | 一个糖精钠分子中有1个臭氧分子 | ||
| C. | 一个糖精钠分子含有17种元素 | D. | 糖精钠的相对分子量质量为183 |
15.对于化学反应:2A=2B+C,反应生成B和C的质量比为B:C=1:8.
此反应为基本反应类型中的分解反应,反应后C的质量是37g.
| 物质 | A | B | C |
| 反应前质量/g | 100 | 0 | 5 |
| 反应后质量/g | 64 |
19.如图所示的变化中,属于化学变化的是( )
| A. | 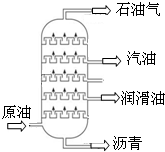 分馏石油 | B. | 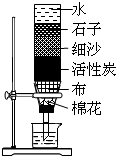 净化水 | ||
| C. |  蒸发食盐水 | D. | 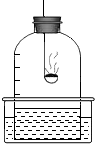 燃烧红磷 |

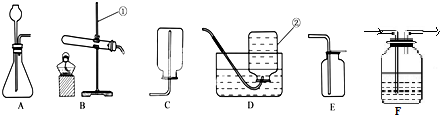

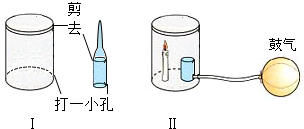 如图所示,实骑室模拟粉尘爆炸实验,连接好装置,在小塑料瓶中放入下列干燥的粉末,点燃蜡烛,快速鼓入大量的空气,能观察到爆炸现象的是B
如图所示,实骑室模拟粉尘爆炸实验,连接好装置,在小塑料瓶中放入下列干燥的粉末,点燃蜡烛,快速鼓入大量的空气,能观察到爆炸现象的是B