题目内容
20.科学知识中有很多的“相等”.请你判断下列说法中正确的是( )| A. | 在化学反应中,反应物的质量总和与生成物的质量总和相等 | |
| B. | 化合物中元素化合价的正价总数与负价总数的数值相等 | |
| C. | 潜水艇在水下潜行时,不管是在深处还是在浅处所受压强相等 | |
| D. | 等质量的金属铁与铝跟等质量且等质量分数的稀硫酸反应生成的氢气质量也一定相等 |
分析 A、根据质量守恒定律分析;
B、根据化合价的原则分析;
C、根据压强定义分析;
D、等质量的金属铁与铝跟足量的等质量分数的稀硫酸反应铝生成的氢气质量多
解答 解:A、根据质量守恒定律可知,参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,注意是“参加反应”,故说法错误;
B、化合物中元素化合价的正价总数与负价总数的数值相等,即化合物中正负化合价的代数和为0,故说法正确;
C、潜水艇所受压强与水的深度有关,深度不同,所受压强不等,故错误;
D、等质量的金属铁与铝跟足量的等质量分数的稀硫酸反应铝生成的氢气质量多,故错误
故选B.
点评 本题考查的知识点多,对学生思维的及时转化是很好的训练.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列说法正确的是( )
| A. | 水壶底部的水垢,可以用NaOH溶液浸泡除去 | |
| B. | 汽车修理工用汽油洗去手上的油污,是乳化作用的 结果 | |
| C. | 增大空气与水的接触面积,不能增大氧气的溶解度 | |
| D. | 析出晶体后的溶液不一定是饱和溶液 |
8.下列应用及相应的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 验证铜的活动性比银强:Cu+2AgCl═CuCl2+2Ag 置换反应 | |
| B. | 盐酸用于除铁锈 Fe2O3+6HCl=2FeCl3+3H2O 复分解反应 | |
| C. | 工业上用高温煅烧石灰石的方法制生石灰:CaCO3═CaO+CO2↑分解反应 | |
| D. | 碳酸钙可作人体补钙剂:CaCO3+H2SO4=CaSO4+H2O+CO2↑ 复分解反应 |
12.铂钯合金在汽车尾气转换过程中加快其化学反应速率,而铂钯合金的质量和化学性质均没有变化,则铂钯合金在反应中是( )
| A. | 氧化剂 | B. | 催化剂 | C. | 还原剂 | D. | 反应物 |
9.图为某一反应的微观示意图,下列说法错误的是( )
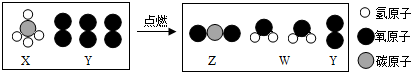

| A. | X是有机物,Z、W是无机物 | |
| B. | 生成物都是氧化物 | |
| C. | 该反应的化学方程式CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O | |
| D. | 点燃X前,要先检验其纯度,以防止爆炸 |
8.化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究.
查得资料:该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成;其他成分遇到盐酸时无气体生成.
方案设计:小组的两位同学提出了各自的设计方案
甲同学:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
乙同学:也利用图示装置进行实验,充分反应后,测定C装置中反应前后的质量差,得出二氧化碳质量,以确定碳酸钙的质量分数.
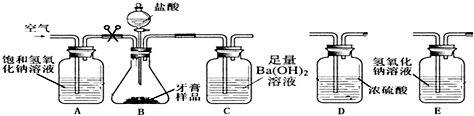
小组同学认为甲同学装置还需要进一步完善,在C装置后他们又增加了一个装置,你认为他们增加的装置是E(选填D或E),其目的是防止空气中的二氧化碳进入C装置影响实验测定.同时小组同学经过讨论后认为乙同学的设计存在明显的缺陷,你认为此缺陷是挥发的氯化氢气体等也进入了C装置.
实验步骤:(1)检查装置气密性(2)打开止水夹,缓缓通入一段时间空气(3)关闭止水夹,打开分液漏斗活塞(4)再次打开止水夹,缓缓通入一段时间空气(5)过滤出沉淀,进行适当的处理后称量其质量.实验过程中,C装置应该在实验步骤2后(填序号)与B装置连接,否则实验结果偏大 (填偏大、偏小或无影响).
进行实验:同学们分四组准确称取四份样品,每份均为16.00g,按照实验步骤分别进行实验,得到了如下的实验数据:
(1)同学们经过讨论后认为第四组同学的数据不正确.造成数据偏差较大的原因可能是BC:
A.实验结束后通入空气速度太快,装置中的二氧化碳没有完全吸收
B.沉淀过滤后没有洗涤
C.沉淀没有干燥直接称量
D.称量沉淀质量时,砝码与药品位置放反了
(2)根据另外三组同学的BaCO3平均质量,计算出了收集到的二氧化碳质量为1.76g.
(3)计算该样品中碳酸钙的质量分数?(写出计算过程)
实验反思:实验后,有同学提出用氢氧化钙溶液替代氢氧化钡溶液可以直接得到碳酸钙沉淀,称量其质量后即可算出质量分数.大家讨论后认为用氢氧化钡溶液比氢氧化钙更好,请说出他们的理由氢氧化钡的溶解性大于氢氧化钙,更容易完全吸收二氧化碳(答出一点即可).
查得资料:该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成;其他成分遇到盐酸时无气体生成.
方案设计:小组的两位同学提出了各自的设计方案
甲同学:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
乙同学:也利用图示装置进行实验,充分反应后,测定C装置中反应前后的质量差,得出二氧化碳质量,以确定碳酸钙的质量分数.

小组同学认为甲同学装置还需要进一步完善,在C装置后他们又增加了一个装置,你认为他们增加的装置是E(选填D或E),其目的是防止空气中的二氧化碳进入C装置影响实验测定.同时小组同学经过讨论后认为乙同学的设计存在明显的缺陷,你认为此缺陷是挥发的氯化氢气体等也进入了C装置.
实验步骤:(1)检查装置气密性(2)打开止水夹,缓缓通入一段时间空气(3)关闭止水夹,打开分液漏斗活塞(4)再次打开止水夹,缓缓通入一段时间空气(5)过滤出沉淀,进行适当的处理后称量其质量.实验过程中,C装置应该在实验步骤2后(填序号)与B装置连接,否则实验结果偏大 (填偏大、偏小或无影响).
进行实验:同学们分四组准确称取四份样品,每份均为16.00g,按照实验步骤分别进行实验,得到了如下的实验数据:
| 组别 | 第一组 | 第二组 | 第三组 | 第四组 |
| 沉淀质量(g) | 7.86 | 7.88 | 7.90 | 9.86 |
A.实验结束后通入空气速度太快,装置中的二氧化碳没有完全吸收
B.沉淀过滤后没有洗涤
C.沉淀没有干燥直接称量
D.称量沉淀质量时,砝码与药品位置放反了
(2)根据另外三组同学的BaCO3平均质量,计算出了收集到的二氧化碳质量为1.76g.
(3)计算该样品中碳酸钙的质量分数?(写出计算过程)
实验反思:实验后,有同学提出用氢氧化钙溶液替代氢氧化钡溶液可以直接得到碳酸钙沉淀,称量其质量后即可算出质量分数.大家讨论后认为用氢氧化钡溶液比氢氧化钙更好,请说出他们的理由氢氧化钡的溶解性大于氢氧化钙,更容易完全吸收二氧化碳(答出一点即可).
 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.