题目内容
(1)随着甲型H1N1病毒的爆发,曾在抗击禽流感斗争中发挥重要作用的达菲胶囊又一次被人们认识和选择.达菲的主要原料--莽草酸,90%来自中国内地.达菲的化学式可表示为C16H36O8N2P,请回答下列问题:
(1)达菲由________种元素组成;达菲中C、H、O元素的质量比为(填最简整数比)________.
达菲中C元素的质量分数为________.(计算结果保留一位小数).
(2)为检验糖尿病患者的尿液,医院要配制8%的CuSO4溶液,现有16g CuSO4固体,可配制该CuSO4溶液________g.配制过程中需要用到的仪器有托盘天平、药匙、胶头滴管、烧杯以及________和________的量筒(从10mL、、1000 mL中选择)
解:(1)由达菲的化学式可知,它由碳、氢、氧、氮和磷这5种元素组成;
其中C、H、O元素的质量比为:12×16:1×36:16×8=48:9:32;
达菲中C元素的质量分数为: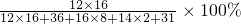 ≈46.3%.
≈46.3%.
故答案为:5;48:9:32;46.3%.
(2)①16g÷8%=200g;
②因为在配制溶液的过程中,需不断搅拌,所以还要用到玻璃棒;
③所要配制的溶液的质量为200g,故选择250 mL的量筒即可.
故答案为:200;玻璃棒;250ml.
分析:(1)根据达菲的化学式可表示为C16H36O8N2P就可知它由几种元素组成,可以计算出C、H、O元素的质量比,利用元素的质量分数公式可以计算出C元素的质量分数;
(2)①根据溶质质量分数公式即可计算出可配制该CuSO4溶液的质量;
②根据配制溶液的实验操作要求即可知道还需什么物品;
③根据所要配制的溶液的质量来选择何时的量筒.
点评:本题主要考查学生运用化学式和溶质质量分数公式进行计算的能力,以及对实验操作的掌握情况.
其中C、H、O元素的质量比为:12×16:1×36:16×8=48:9:32;
达菲中C元素的质量分数为:
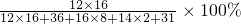 ≈46.3%.
≈46.3%.故答案为:5;48:9:32;46.3%.
(2)①16g÷8%=200g;
②因为在配制溶液的过程中,需不断搅拌,所以还要用到玻璃棒;
③所要配制的溶液的质量为200g,故选择250 mL的量筒即可.
故答案为:200;玻璃棒;250ml.
分析:(1)根据达菲的化学式可表示为C16H36O8N2P就可知它由几种元素组成,可以计算出C、H、O元素的质量比,利用元素的质量分数公式可以计算出C元素的质量分数;
(2)①根据溶质质量分数公式即可计算出可配制该CuSO4溶液的质量;
②根据配制溶液的实验操作要求即可知道还需什么物品;
③根据所要配制的溶液的质量来选择何时的量筒.
点评:本题主要考查学生运用化学式和溶质质量分数公式进行计算的能力,以及对实验操作的掌握情况.

练习册系列答案
相关题目
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 35 | 8 | 2 | 5 |
| 反应后质量/g | 待测 | 1 | 42 | 3 |
- A.该反应属于化合反应
- B.该反应中X与Z是生成物
- C.该反应后X待测值为4
- D.该反应后生成42g Z物质
 珍珠粉以其良好的养颜等功效,获得消费者喜爱.资料显示:珍珠中含碳酸钙80-93%、蛋白质4-14%、水份2-4%、十几种氨基酸、28种微量元素.然而一些不法分子用回收的贝壳加上工业用氢氧化钠配制的药水进行清洗、晾晒以后直接加工销售,其主要成分是:碳酸钙,及少量残留氢氧化钠.以下是某化学兴趣小组设计辨别真假珍珠,并测定珍珠中碳酸钙含量的实验探究方案.
珍珠粉以其良好的养颜等功效,获得消费者喜爱.资料显示:珍珠中含碳酸钙80-93%、蛋白质4-14%、水份2-4%、十几种氨基酸、28种微量元素.然而一些不法分子用回收的贝壳加上工业用氢氧化钠配制的药水进行清洗、晾晒以后直接加工销售,其主要成分是:碳酸钙,及少量残留氢氧化钠.以下是某化学兴趣小组设计辨别真假珍珠,并测定珍珠中碳酸钙含量的实验探究方案.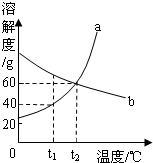 如图是a、b两种固体物质的溶解度曲线.T1℃时,在两个烧杯中分别加入a、b两种物质各60 g后,再分别加入100 g水,充分搅拌.下列叙述正确的是
如图是a、b两种固体物质的溶解度曲线.T1℃时,在两个烧杯中分别加入a、b两种物质各60 g后,再分别加入100 g水,充分搅拌.下列叙述正确的是