题目内容
13.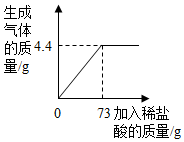 某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图所示
某品牌纯碱中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取12g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图所示(1)计算该样品中含杂质的质量分数是多少?(计算结果保留一位小数,下同)
(2)计算当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是多少?
分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据提供的数据和反应的化学方程式可以进行相关方面的计算和判断.
解答 解:(1)设碳酸钠质量为x,反应生成氯化钠质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 4.4g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{4.4g}$,
x=10.6g,y=11.7g,
该样品中含杂质的质量分数是:$\frac{12g-10.6g}{12g}$×100%=11.7%,
答:该样品中含杂质的质量分数是11.7%.
(2)当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是:$\frac{12g-10.6g+11.7g}{12g+73g-4.4g}$×100%=16.3%,
答:当盐酸与纯碱恰好完全反应时,所得溶液的溶质质量分数是16.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
4. 某科学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量.先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品,开始计时,并将电子天平的读数记录在表中,请回答下列问题:
某科学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量.先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品,开始计时,并将电子天平的读数记录在表中,请回答下列问题:
(1)完全反应后,产生氢气的质量是0.4g.
(2)合金中铁元素的质量百分含量为多少?
(3)完全反应后,烧杯中溶液的质量是多少?
 某科学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量.先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品,开始计时,并将电子天平的读数记录在表中,请回答下列问题:
某科学兴趣小组使用如图所示装置,对某种铁铜合金的成分进行测量.先取足量稀硫酸于烧杯中,再向其中加入14.0g合金样品,开始计时,并将电子天平的读数记录在表中,请回答下列问题:| 空烧杯 | 加硫酸后 | 加样品后 5分钟 | 加样品后 12分钟 | 加样品后 21分钟 | 加样品后 40分钟 | 加样品后 3小时 | |
| 读数(g) | 28.5 | 169.7 | 183.6 | 183.5 | 183.4 | 183.3 | 183.3 |
(2)合金中铁元素的质量百分含量为多少?
(3)完全反应后,烧杯中溶液的质量是多少?
1.化石燃料燃烧会排放大量的二氧化碳,引起温室效应,一种新的处理方法是将二氧化碳气体通入含有长石(主要成分KAlSi3O8)的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O═KHCO3+X+3SiO2↓,下列说法不正确的是( )
| A. | X是Al(OH)3 | |
| B. | 反应前后各物质中元素的化合价均未发生变化 | |
| C. | 生成物中有一种氧化物 | |
| D. | 该反应中涉及到的元素种类有5种 |
8.下列变化中,属于化学变化的是( )
| A. | 食物腐烂 | B. | 滴水成冰 | C. | 美酒飘香 | D. | 水果榨汁 |
3.依据所给食物的近似pH判断,下列说法正确的是( )
| 食物 | 白葡萄汁 | 苹果 | 牛奶 | 玉米粥 |
| pH | 3.5-4.5 | 2.9-3.3 | 6.3-6.6 | 6.8-8.0 |
| A. | 苹果汁和葡萄汁显酸性 | B. | 葡萄汁的酸性比苹果汁强 | ||
| C. | 玉米粥和牛奶显碱性 | D. | 胃酸过多的人不宜常喝玉米粥 |