题目内容
15.氨气(NH3)是一种无色有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,显碱性.氨气在化学工业中用途很广泛,例如制化肥、制纯碱等.近年来,氨气还用于环境治理.(1)“候氏制碱法”的两步主要反应原理可表示为
Ⅰ.NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl,
Ⅱ.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.其中,NaHCO3属于 ①盐(“酸”、“碱”或“盐”),此反应属于 ②分解反应,Na2CO3的俗名叫 ③纯碱或苏打.
(2)在细菌作用下,用氨处理含甲醇的工业废水,使其变为无毒的N2和CO2,从而清除对环境的污染,有关的反应为:6NH3+5CH3OH+12B═3N2↑+5CO2↑+19H2O,其中B物质的化学式是O2.
(3)氨气可以被硫酸吸收,生成可以用作氮肥的硫酸铵,该反应的化学方程式为:2NH3+H2SO4═(NH4)2SO4.若用盐酸吸收氨气,则反应的化学方程式为:NH3+HCl=NH4Cl.
分析 (1)根据化学式的特点分析物质的属类;根据基本的反应类型结合反应物和生成物的特点分析;根据碳酸钠的俗名回答;
(2)根据质量守恒定律中反应前后原子的种类、个数不变分析B的化学式;
(3)根据氨气和硫酸的反应写出方程式.
解答 解:(1)碳酸氢钠是由金属离子和酸根离子构成的化合物,因此NaHCO3属于盐;反应②是一种物质生成三种物质的分解反应;碳酸钠俗名纯碱或苏打;故答案为:盐;分解;纯碱或苏打;
(2)由化学方程式可知,反应物氮、氢、碳、氧原子个数分别为6、38、5、5,反应后的生成物中氮、氢、碳、氧原子个数分别为6、38、5、29,根据反应前后原子种类、数目不变,则12B中含有24个氧原子,则每B分子由2个氧原子构成,则物质B的化学式为O2;故答案为:O2;
(3)氨气和硫酸的反应生成硫酸铵,则氨气和盐酸反应产生氯化铵,反应的方程式为:NH3+HCl=NH4Cl;故答案为:NH3+HCl=NH4Cl.
点评 本题难度不大,掌握利用化学式给物质分类、常见物质的俗名、反应类型的判断、利用原子守恒来确定物质的化学式的方法、化学方程式的书写是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.含碳元素的物质是化学世界中最庞大的家族,请填写下列空格:
(1)在学习化学的过程中我们认识的①一氧化碳、②碳酸、③碳酸钙、④二氧化碳,都是碳家族的成员.
其中(请选择上述物质的编号填空):
可乐中含有的一种酸是②;用于冶炼金属的氧化物①;引起温室效应的是④.
(2)根据下表提供的信息,填写有关含碳物质的对应特征.
(3)液态二氧化碳灭火器可用于扑灭档案资料室发生的火灾,下列说法不正确的是A、B(填标号)
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物的着火点.
(1)在学习化学的过程中我们认识的①一氧化碳、②碳酸、③碳酸钙、④二氧化碳,都是碳家族的成员.
其中(请选择上述物质的编号填空):
可乐中含有的一种酸是②;用于冶炼金属的氧化物①;引起温室效应的是④.
(2)根据下表提供的信息,填写有关含碳物质的对应特征.
| 物质用途 | 金刚石切割玻璃 | 石墨做电极 | 活性炭净水 |
| 对应特性 | ①硬度大 | ②优良的导电性 | ③吸附性 |
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物的着火点.
 儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答:
儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答: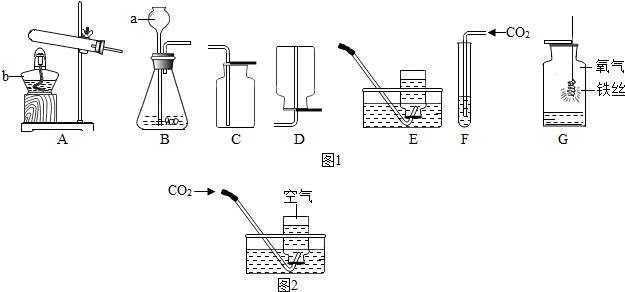
 如图是实验室里制取二氧化碳的一种发生装置:
如图是实验室里制取二氧化碳的一种发生装置: 石灰石是我省的主要矿产之一,其主要成分碳酸钙(CaCO3)高温煅烧可制得氧化钙(CaO)和二氧化碳(杂质不参加反应).学习小组为了测定当地矿山石灰石中碳酸钙的含量,将16g石灰石高温煅烧,测得的相关数据如图,试回答:
石灰石是我省的主要矿产之一,其主要成分碳酸钙(CaCO3)高温煅烧可制得氧化钙(CaO)和二氧化碳(杂质不参加反应).学习小组为了测定当地矿山石灰石中碳酸钙的含量,将16g石灰石高温煅烧,测得的相关数据如图,试回答: