题目内容
(6分)能源、环境与人类的生活和社会发展密切相关。
(1)目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和 。
(2)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如下所示:
①该反应的基本反应类型为 。
②该反应生成物的分子个数比为 。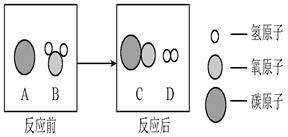
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现 燃烧的产物没有污染,且释放大量能量,有一定应用前景。
燃烧的产物没有污染,且释放大量能量,有一定应用前景。
① 中氮元素和氢元素的质量比为 。(2分)
中氮元素和氢元素的质量比为 。(2分)
②将 燃烧反应的化学方程式补充完整:
燃烧反应的化学方程式补充完整: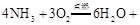 。
。
(1)天然气 C+H2O=CO+H2
(2)①置换反应 ②1:1
(3)①14:3 ②4NH3+3O2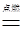 6H2O+2N2
6H2O+2N2
解析试题分析:(1)化石燃料亦称矿石燃料,它们是古代生物遗体在特定地质条件下经过一系列复杂变化形成的复杂的混合物,主要包括煤、石油和天然气等天然资源。
(2)根据微粒的微观模拟示意图可知,A为C,B为H2O,C为CO,D为H2;故该反应的化学方程式为H2O+C=CO↑+H2↑。
①该反应是一种单质和一种化合物反应,生成另一种单质和另一种化合物的置换反应;
②根据H2O+C=CO↑+H2↑可知,该反应中生成物的分子个数比为1:1。
(3)①元素的质量比为相对原子质量乘以原子个数之比,所以NH3中氮元素和氢元素的质量比=14:3;
②由于反应物中有4个氮原子、12个氢原子、6个氧原子;而生成物中有12个氢原子,6个氧原子,根据质量守恒定律(原子种类、个数不变)可知,生成物中少4个氮原子,所以另一种生成物是氮气,方程式为4NH3+3O2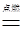 6H2O+2N2。
6H2O+2N2。
考点:化石燃料及其综合利用,微粒观点及模型图的应用,元素质量比的计算,反应类型的判定,质量守恒定律及其应用
点评:分子是由原子构成的,且同种原子构成的分子是单质分子,不同种原子构成的分子是化合物分子。试题通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力,以检测考生从微观角度认识化学的意识和能力。

 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案