题目内容
4.下列实验操作中,正确的是( )| A. |  吸取液体 | B. |  倾倒液体 | C. |  浊液过滤 | D. |  蒸发结晶 |
分析 A、根据胶头滴管的使用方法进行分析判断.
B、根据向量筒中倾倒液体药品的方法进行分析判断.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据蒸发操作的注意事项进行分析判断.
解答 解:A、使用胶头滴管时,伸入液体前,应捏紧胶头,排出里面的空气,再伸入试剂中吸取液体,图中液体中有气泡产生,说明伸入液体前没有捏紧胶头排出里面的空气,图中所示操作错误.
B、向量筒中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示操作正确.
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误.
D、正在加热的蒸发皿温度较高,为防止烫伤手,不能用手直接拿热的蒸发皿,应用坩埚钳夹取,图中所示操作错误.
故选:B.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
12.某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如图1所示的实验方案.
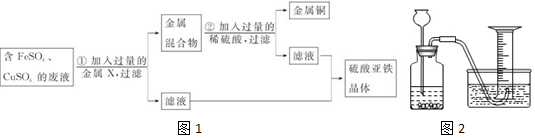
(1)结合实验方案回答下列问题:
步骤①中,金属X是铁,该反应的化学方程式为Fe+CuSO4═FeSO4+Cu;
步骤②中,加入过量稀硫酸的目的是使铁完全反应;
(2)为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小吴设计了一套实验装置(如图2),他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量和质量分数)进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如表:
(1)由实验结果可知:金属活动性较强的是乙.
(2)为了使得到的实验数据准确,小吴开始收集气体的时间点应该是A.
A.导管口一有气泡冒出时
B.冒出气泡连续且均匀时
C.检验产生的气体纯净时
(3)根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道B.
A.参加反应的硫酸质量
B.生成物中金属元素的化合价.

(1)结合实验方案回答下列问题:
步骤①中,金属X是铁,该反应的化学方程式为Fe+CuSO4═FeSO4+Cu;
步骤②中,加入过量稀硫酸的目的是使铁完全反应;
(2)为了比较甲、乙两种金属的活动性强弱和相对原子质量大小,小吴设计了一套实验装置(如图2),他取两种金属(表面积相同)各m克,分别加入足量的稀硫酸(相同质量和质量分数)进行反应,在相同条件下测定不同时间内收集到的气体体积,实验记录如表:
| 反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
| 收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
| 乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 | |
(2)为了使得到的实验数据准确,小吴开始收集气体的时间点应该是A.
A.导管口一有气泡冒出时
B.冒出气泡连续且均匀时
C.检验产生的气体纯净时
(3)根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道B.
A.参加反应的硫酸质量
B.生成物中金属元素的化合价.
19.下列实验方法不能达到目的是( )
| A. | 鉴别硬水和软水-用肥皂水 | |
| B. | 鉴别CuO粉、铁粉-用稀硫酸 | |
| C. | 除去CaO中的CaCO3-高温煅烧 | |
| D. | 除去FeSO4溶液中的CuSO4-加足量锌,过滤 |
9.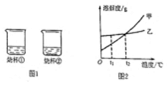 将等质量的甲、乙两种固体分别放在两个烧杯中,向两个烧杯中分别加入等质量的t1℃的水、搅拌、静置,一段时间后烧杯中的现象如图1所示.图2是甲、乙的溶解度曲线图,下列说法正确的是( )
将等质量的甲、乙两种固体分别放在两个烧杯中,向两个烧杯中分别加入等质量的t1℃的水、搅拌、静置,一段时间后烧杯中的现象如图1所示.图2是甲、乙的溶解度曲线图,下列说法正确的是( )
 将等质量的甲、乙两种固体分别放在两个烧杯中,向两个烧杯中分别加入等质量的t1℃的水、搅拌、静置,一段时间后烧杯中的现象如图1所示.图2是甲、乙的溶解度曲线图,下列说法正确的是( )
将等质量的甲、乙两种固体分别放在两个烧杯中,向两个烧杯中分别加入等质量的t1℃的水、搅拌、静置,一段时间后烧杯中的现象如图1所示.图2是甲、乙的溶解度曲线图,下列说法正确的是( )| A. | 烧杯②中盛放的一定是乙 | |
| B. | 烧杯①中的溶液一定是不饱和溶液 | |
| C. | 将两烧杯中的溶液混合后,烧杯中一定有固体剩余 | |
| D. | 若水不蒸发,两烧杯内溶液升温到t2℃时某质量分数一定相等 |
14.向AgNO3和Cu(NO3)2的混合溶液中加入一定质量锌,完全反应后过滤,得滤渣和滤液,下列情形中有可能出现的是( )
| A. | 向滤渣中滴稀盐酸时有气泡产生,滤液中只含Zn(NO3)2 | |
| B. | 向滤渣中滴稀盐酸时无气泡产生,滤液中只含AgNO3和Zn(NO3)2 | |
| C. | 向滤液中滴稀盐酸时有白色沉淀产生,滤渣中一定含有Ag和Cu | |
| D. | 向滤液中滴加稀盐酸时无白色沉淀产生,滤渣中一定含Ag和Zn |
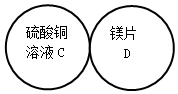 用四个圆表示A(铁片)、B(稀硫酸)、C(硫酸铜溶液)、D(镁片)四种物质,用两圆相切表示两种物质可以发生反应,如图所示.请回答下列问题:(提示:物质间均恰好完全反应,其中稀硫酸与硫酸铜溶液不反应)
用四个圆表示A(铁片)、B(稀硫酸)、C(硫酸铜溶液)、D(镁片)四种物质,用两圆相切表示两种物质可以发生反应,如图所示.请回答下列问题:(提示:物质间均恰好完全反应,其中稀硫酸与硫酸铜溶液不反应) 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的纯碱溶液,请在图中画出溶液的pH随滴入纯碱的量的大概变化图象,并解释各段变化的理由.
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的纯碱溶液,请在图中画出溶液的pH随滴入纯碱的量的大概变化图象,并解释各段变化的理由.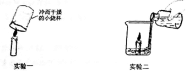 如图是有关蜡烛燃烧的两个实验,请回答有关问题.
如图是有关蜡烛燃烧的两个实验,请回答有关问题.