题目内容
20.X、Y、Z在常温下是三种金属固体,将X浸入稀硫酸中,Y溶解并产生氢气,X无变化,将X和Z浸入硝酸银溶液中,X表面有银析出而Z无变化①判断Z在金属活动性顺序表中的位置
②具体确定一种X后,描述X与硝酸银溶液反应的现象.
分析 根据金属活动性顺序的意义进行分析,在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答 解:Y能与稀H2SO4反应而X不能,推知Y的活动性大于X的活动性并且X位于H后面;由“X和Z浸入AgNO3溶液中,X表面有Ag析出而Z无变化”推知:X的活动性大于Ag,而Z的活动性小于Ag,综上所述则有Y>H>X>Ag>Z,选用的X,其活动性要排在H与Ag之间即可,如Cu、Hg等;如果X为铜;方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag,现象为:铜的表面附着着银白色固体,溶液由无色变成蓝色;
故答案为:①X活动性要排在H与Ag之间;
②如果X为铜,现象为:铜的表面附着着银白色固体,溶液由无色变成蓝色.
点评 解答本题关键是要知道叙述实验现象时要根据生成物的颜色和状态考虑.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
10.因汽油价格上调,杭州市区内的士费用外加1元,但这并不意味着机动车的燃料危机已经解除.下列缓解机动车燃料危机的设想不合理的是( )
| A. | 使用乙醇汽油 | |
| B. | 改进发动机的燃烧方式,使汽油充分燃烧 | |
| C. | 从植物中提炼汽油 | |
| D. | 寻找新的催化剂使水变汽油 |
11.下列各选项中前者是纯净物,后者是混合物的是( )
| A. | 氢氧化钠 稀盐酸 | B. | 碘酒 碘化钾 | ||
| C. | 空气 氧气 | D. | 海水 石灰水 |
15.下列图象分别于选项中的操作相对应,其中不合理的是( )
| A. | 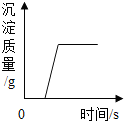 向一定量的盐酸和CaCl2混合溶液中的第如Na2CO3溶液 | |
| B. | 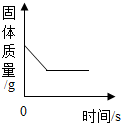 加热氯酸钾和二氧化锰的混合物 | |
| C. | 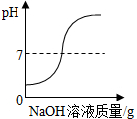 向一定量的盐酸中滴入NaOH溶液 | |
| D. | 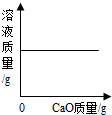 一定温度时,向一定量的饱和石灰水中加入生石灰 |
5.下列图象关系合理的是( )
| A. |  加热一定质量的氯酸钾和二氧化锰的混合固体 | |
| B. |  电解水 | |
| C. |  一定温度下,向饱和氯化钠溶液中加入硝酸钾 | |
| D. |  向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的质量关系 |
9.某仓库工作人员违章操作,在雨天转运“保险粉”引起爆炸.“保险粉”化学名为连二亚硫酸钠(Na2S2O4),主要用于印染工业.该化学品在潮湿空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4=Na2S2O3+Na2SO3+X.下列有关说法正确的是( )
| A. | X的化学式为SO3 | |
| B. | 该反应中硫元素和氧元素的化合价发生了变化 | |
| C. | Na2S2O4需要干燥密闭储存 | |
| D. | 该分解反应是个吸热的反应 |
 人类的生产、生活离不开金属.
人类的生产、生活离不开金属.